von Fred Gardner und Dr. John McPartland.
Wir können uns nur vorstellen, wie die Menschen vor Tausenden von Jahren entdeckt haben, dass eine bestimmte Pflanze heilende Eigenschaften hat. Vielleicht sammelte eine Frau Samen, um sich zu ernähren, als eine schmerzhafte Periode einsetzte. Als sie die Samen aus den Blütenspitzen der Pflanze löste, klebte ein klebriges Harz an ihren Händen. Sie knabberte ein wenig von der gummiartigen Substanz ab. Bald darauf ging es ihr besser.
Ihre Freunde bestätigten, dass es sich tatsächlich um eine krampflösende Pflanze handelte. Sie begannen, sie absichtlich anzubauen. Als ihr Stamm weiterzog, brachten sie Samen mit, um sie in der nächsten Siedlung in den Boden zu stecken. Ähnliche Entdeckungen müssen viele Male in vielen Gruppen gemacht worden sein. Die Menschen erkannten, dass die Samen nahrhaft waren, das Harz schmerzlindernd wirkte und der Stängel Fasern für Seile und Netze lieferte.
Hier und da begannen Stämme, diese besonders nützliche Pflanze gezielt anzubauen. Die Einzelheiten sind im Nebel der Geschichte verloren gegangen, aber die Pflanze ist geblieben und den Botanikern heute als Cannabis bekannt . (Der lateinische Name der Pflanze ist kursiv geschrieben, Cannabis, das Produkt, das aus der Pflanze hergestellt wird, hingegen nicht)
Cannabis hat sich lange vor dem Menschen entwickelt, aber da niemand Cannabis-Makrofossilien in Gesteinen gefunden hat, ist es schwer zu sagen, wann. Zwei DNA-Studien gehen davon aus, dass sich Cannabis entweder vor 21 oder 27,8 Millionen Jahren entwickelt hat. Versteinerter Pollen, der als Cannabis identifiziert wurde, stammt aus der Zeit vor 787.000 Jahren in Südsibirien.
Jüngerer Pollen, etwa 125.000 Jahre alt, wurde aus einem sibirischen Moor gewonnen. Knochen von Neandertalern aus der gleichen Zeit wurden in einer 30 Meilen entfernten Höhle gefunden. Einige Zeit nachdem der Homo sapiens vor 40.000 Jahren in die Region eingewandert war, gingen wir eine Partnerschaft mit der Pflanze ein.
„Hanf folgte dem Menschen auf natürliche Weise“, schrieb Nicolai Vavilov, der große russische Pflanzenforscher, „er hielt sich in der Nähe seiner Behausungen auf, siedelte sich auf Abfällen und überall dort an, wo der Boden gedüngt wurde.“ Edgar Anderson, ein bekannter Botaniker der Harvard University und des Missouri Botanical Garden, machte das Bild des Hanfes als „Mitläufer“ populär.
Irgendwann begannen die Menschen, die Pflanzen mit den Eigenschaften auszuwählen, die sie für den Anbau schätzten – hohe Stängel, große ölige Samen oder heilendes, psychoaktives Harz. Vavilov, Anderson, Carl Sauer, Andrew Sherratt und Carl Sagan haben die Ursprünge der Landwirtschaft mit den Bemühungen unserer Vorfahren in Verbindung gebracht, nützliches Cannabis anzubauen. Sauer schlug vor, dass die Landwirtschaft von Menschen entwickelt wurde, die in Fischereigemeinschaften an Flüssen und Seen lebten (dem Lebensraum von „Ditchweed“) und begannen, die Pflanzen als Quelle für Angelschnüre und Netze anzubauen. Niemand weiß genau, wo und wann.

Cannabisanbau im Rif-Gebirge, Marokko
Klassifizierung
Der schwedische Botaniker Carl Linnaeus beschrieb Cannabis sativa offiziell im Jahr 1753. Zweiunddreißig Jahre später identifizierte Jean Baptiste Lamarck Cannabis indica als eine zweite Art. Experten streiten immer noch darüber, ob sie als separate Arten oder als separate Sorten einer Art klassifiziert werden sollten. Bei den noch existierenden Populationen einer möglichen dritten Art, Cannabis ruderalis, könnte es sich um einen Wildtyp handeln, der vom Vorfahren von C. sativa abstammt .
Dann kam That ’70s Show, als die Cannabis-Taxonomie in das US-Rechtssystem verwickelt wurde. Der Ethnobotaniker Richard Evans Schultes, ein Zeuge der Verteidigung, behauptete, dass sich die Betäubungsmittelgesetze auf C. sativa beziehen, während der Angeklagte C. indica besaß, die gesetzlich übersehen wurde und technisch legal war. Ernest Small, ein taxonomischer Botaniker, plädierte im Namen der Kläger für eine einzige Art.
Leider nahmen Schultes und sein Kollege Loren Anderson subtile Veränderungen in der Cannabis-Taxonomie vor, die von den ursprünglichen Konzepten von Linnaeus und Lamarck abwichen. Sie schlossen sowohl Drogenpflanzen als auch Faserpflanzen in C. sativa ein . (Heute wissen wir, dass die Drogenpflanzen reich an 9-Tetrahydrocannabinol oder THC sind und die Faserpflanzen reich an Cannabidiol oder CBD) William Stern untersuchte 1974 die C. sativa-Exemplare von Linnaeus und stellte fest, dass es sich um „alte Kulturhanfbestände aus Nordeuropa“ handelte – also um Hanfpflanzen, die CBD enthalten, nicht um Drogenpflanzen.

Der Naturschützer und Hanfaktivist David Bronner, Präsident von Dr. Bronner’s Magic Soaps, begutachtet ein Feld mit Industriehanf in Colorado, 2013. Siehe www.drbronner.com für weitere Informationen.
Schultes und Anderson beschränkten C. indica auf Pflanzen, die Schultes in Afghanistan gesehen hat. So charakterisierten sie „indica“ als kurze, dicht verzweigte Pflanzen mit breiten Fiederblättern und „sativa“ in Anlehnung an Lamarcks Arten – hoch, locker verzweigt, mit schmalen Fiederblättern. Daraus entstand die umgangssprachliche Taxonomie von „sativa“ und „indica“, die bis heute gebräuchlich ist. Mit dem wachsenden Interesse an Pflanzen mit hohem CBD-Gehalt, von denen einige C. sativa im Linnae’schen Sinne sind, ist die umgangssprachliche Taxonomie wirklich verworren geworden.
Der Botaniker Karl Hillig trennt diese Populationen voneinander: C. sativa steht für CBD-dominante Pflanzen aus Europa, die entweder kultiviert werden(C. sativa Hanf-Biotyp) oder wild wachsen(C. sativa Wildtyp).
C. indica steht für THC-dominante Pflanzen aus Asien, entweder Lamarcks Pflanzen aus Indien – C. indica NLD („narrow leaflet diameter“, im Volksmund „sativa“ genannt) oder Pflanzen aus Afghanistan – C. indica WLD („wild leaflet diameter“, im Volksmund „indica“ genannt).
Die Naturforscher Robert Clarke und Mark Merlin übernahmen Hilligs System und erweiterten es. Bei der Untersuchung der weltweiten Verbreitung von Cannabispflanzen – wild, kultiviert und verwildert (einmal kultiviert, wieder wild) – kommen diese Experten zu dem Schluss:
Schmalblättriger Hanf, C. sativa, Unterart sativa, wurde vor allem in Europa angebaut.
Breitblättriger Hanf, C. indica, Unterart chinensis, wurde in China, Korea, Japan und Südostasien angebaut.
Schmalblättrige Drogenpflanzen, C. indica, Unterart indica, wurden in Süd- und Südostasien und im Nahen Osten angebaut.
Breitblättrige Drogenpflanzen, C. indica, Unterart afghanica, wurden in Nordafghanistan und Pakistan angebaut.
Beachte, dass die weit verbreitete Kreuzung und Hybridisierung von schmal- und breitblättrigen Pflanzen die Anwendung dieser Begriffe in vielen Fällen botanisch ungenau gemacht hat.
Medizinische Verwendung vor der Neuzeit
Alle berühmten Wiegen der Zivilisation in der Alten Welt haben Cannabis medizinisch genutzt – China, Mesopotamien, Griechenland, Indien und vielleicht Ägypten. Die Skythen, ein Migrantenstamm, der Cannabisdampf zu rituellen Zwecken inhalierte, wanderten um 800 v. Chr. aus ihrer sibirischen Heimat aus. Sie hatten keine Schriftsprache, aber ihr Wort für Cannabis wurde als kanab, kanap, konaba oder kannabis rekonstruiert. Die Skythen beeinflussten die Zivilisationen in China, Indien und Mesopotamien an der Schwelle zur Geschichte.
Der Arzt und Historiker Ethan Russo hat ein Grab auf dem Friedhof von Yánghai besucht, das fast ein Kilo Cannabis enthielt. Es war grob manipuliert – Blütenspitzen, Blätter und Samen, aber keine Stängel. Das Grab enthielt keine Hanffasern. Es wird auf 766-416 v. Chr. datiert. In der Nähe sind Skythen begraben. Yánghai liegt im Turpan-Becken, das heute zu China gehört.
Die alten Chinesen kannten Cannabis als „má“ Ihr Piktogramm für má stellt zwei Pflanzen dar, die kopfüber zum Trocknen aufgehängt wurden. Die Kombination von má mit dem Zeichen yào (Droge) bedeutet „Narkotikum“ oder „Betäubungsmittel“
Der legendäre Arzt Shénnóng schreibt in seinem daoistisch geprägten Medizinbuch Shénnóng Ben Cao Jing (auch bekannt als Pen Ts’ao Ching) ausführlich über má. Er warnt: „Wenn man viel davon einnimmt, kann man Geister sehen und frenetisch herumlaufen. Bei längerer Einnahme kann man mit dem Geist kommunizieren und den Körper leicht machen.“ Shénnóng soll vor etwa 4000 Jahren gelebt haben, aber die legendäre Existenz des Mannes blieb bis etwa 130 v. Chr. unerwähnt.
Die Skythen gingen in die Geschichte ein, als sie während der Herrschaft von König Sargon II (722 705 v. Chr.) in Mesopotamien einfielen. Nachdem die Skythen in Assyrien eingefallen waren, tauchte ein neues Wort in der neuassyrischen Keilschrift auf. Das Wort, das „Hanf“ bedeutet, wird als qunubu oder qunnabu transliteriert. Das Wort taucht in Zusammenhängen auf, die auf die Verwendung durch Schamanen hindeuten, was die Verbindung zu den Skythen noch verstärkt.

Das chinesische Piktogramm „má“ steht für Cannabis – zwei Pflanzen, die kopfüber zum Trocknen aufgehängt wurden.

Die Hindu-Gottheit Shiva wird seit langem mit Cannabis in Verbindung gebracht.
Herodot, der griechische „Vater der Geschichte“, schrieb um 440 v. Chr. ausführlich über die Skythen. Herodot prägt das Wort xávvaßiç von einem Wort, das er von den Skythen übernommen hat . Er beschrieb, wie sie xávvaßiç für Tauwerk und Stoffe verwendeten und xávvaßiç in kleinen Zelten verdampften.
In Indien gibt es mehr als 50 Wörter für Cannabis und Cannabisprodukte. Archäologen haben im Einzugsgebiet des Ganges Cannabissamen ausgegraben, die mindestens aus dem Jahr 1300 v. Chr. stammen. Im Atharvaveda, der um 900 v. Chr. verfasst wurde, wird eine Pflanze, von der viele Experten annehmen, dass es sich um Cannabis handelt, bhånga genannt. Diese Daten liegen vor der Ankunft der Skythen, deren früheste Anwesenheit am Hindukusch auf das siebte Jahrhundert vor Christus datiert werden kann.
Siddhartha Gautama (ca. 563-483 v. Chr.), der Buddha unserer historischen Zeitrechnung, war ein Indo-Skythen. Angeblich ernährte er sich während seiner sechs Stufen der Askese von einem Hanfsamen pro Tag. Praktiker der ayurvedischen Medizin, dem traditionellen indischen System, empfehlen das Kraut gegen Schmerzen, Schlaflosigkeit und Appetitlosigkeit.
Die ägyptische Hieroglyphe šmšmt wurde als Cannabis gedeutet. Das Wort taucht in den Pyramidentexten von 2350 v. Chr. auf, „die Schnüre (oder Seile) der šmšmt-Pflanze “ Allerdings war Flachs und nicht Hanf die wichtigste Faserpflanze im alten Ägypten. Andere Autoren interpretieren šmšmt als Corchorus olitorius, ein faseriges Kraut, dessen Blätter in Ägypten gegessen und medizinisch verwendet werden. Das Wort ähnelt auch šmšm, dem arabischen Wort für Sesam. Gute Belege für Cannabis in Ägypten stammen aus der Römerzeit.
Die bekannte polnische Anthropologin Sara Benet (neé Benetowa) behauptet, dass kaneh bosm (qaneh bosem) im Alten Testament, Exodus 30:22-25, Cannabis bedeutet. Das Wort wird normalerweise mit „aromatisches Rohr“ übersetzt Mose verwendete kaneh bosm für ein heiliges Salböl. Benetowa stellt „die erstaunliche Ähnlichkeit“ zwischen dem semitischen kanbos und dem skythischen Wort für Cannabis fest. Aber das Buch Exodus wurde im 8. oder 9. Jahrhundert v. Chr. verfasst, und die Skythen fielen erst 630 v. Chr. in das Land Israel ein. Zu diesem Zeitpunkt waren die Israeliten bereits verstreut und von den Assyrern vertrieben worden.
Cannabis ist im Fruchtbaren Halbmond nicht heimisch. Kanbos, das auch als kanbus oder qannabbôs transliteriert wird, erscheint erstmals in der Mischna, die im 1.
Jahrhundert v. Chr. geschrieben wurde. Angesichts der Beweise, dass Cannabisprodukte in der Antike zur Behandlung von Krankheiten weit verbreitet waren, ist es ein echtes Rätsel, warum die Pflanze in Ungnade fiel – ein historisches Phänomen, das Ethan Russo „Cannabis interruptus“ nannte Auf der Suche nach einer Erklärung führt Russo „die Vergänglichkeit“ der historischen Aufzeichnungen und „die Neigung der Menschheit zu ständigen Kriegen, Invasionen und kulturellen Konflikten“ an
Es ist, als hätte es in jeder Gesellschaft schon immer Prohibitionisten gegeben, die sich von Zeit zu Zeit gegen die Ärzte und Patienten durchsetzen, die Cannabisprodukte sinnvoll einsetzen. Eine Theorie besagt, dass in vielen Kulturen Angehörige der Priesterklasse psychoaktive Pflanzen als Bedrohung für ihre Rolle als Vermittler zwischen der materiellen und der spirituellen Welt ansahen. Sie wollten nicht, dass Menschen ohne ihre Aufsicht Visionen und kreative Einsichten haben. In der heutigen Zeit ist die Prohibition von Cannabis eine effektive Methode der sozialen Kontrolle – ein Mechanismus zur Finanzierung und Bewaffnung der Polizei und ein Marker für Ungehorsam in der Bevölkerung.
Das Muster, dass Cannabis sich als medizinisch nützlich erwies, aber verboten wurde, setzte sich in verschiedenen Teilen der Welt während des Mittelalters fort. Im islamischen Ägypten, so Russo, „spotteten zwar viele über die psychoaktiven Wirkungen von Cannabis, weil die muslimische Scharia Rauschmittel verbot, aber die zahlreichen medizinischen Eigenschaften wurden häufig neidlos anerkannt.“
Ein ägyptischer König erließ im 13. Jahrhundert ein Verbot, aber als Napoleon 1798 in Ägypten einmarschierte, war der Gebrauch des Krauts weit verbreitet und die Franzosen sahen sich veranlasst, ein eigenes Verbot auszusprechen. Dreißig Jahre später berichtete der französische Arzt Aubert-Roche, dass Cannabis während eines Pestausbruchs in Alexandria Fieber, Unruhe, Schmerzen, Bronchitis und Schlaflosigkeit linderte. Und so schwang das Pendel weiter zwischen Verboten und Verschreibung.
Cannabis in der medizinischen Literatur
Wie Frankreich entdeckte auch England das medizinische Cannabis über seine Kolonien. Die Nachricht wurde von einem brillanten, in Irland geborenen und in Edinburgh ausgebildeten Arzt namens William Brooke O’Shaughnessy überbracht. Die British East India Company schickte O’Shaughnessy in den 1830er Jahren nach Kalkutta. Er war ein junger Star, der bereits für die Entwicklung einer wirksamen Cholera-Behandlung – der Elektrolyt-Ersatztherapie – bekannt war, aus der sich die intravenöse Verabreichung von Medikamenten entwickeln sollte.
In Indien beobachtete O’Shaughnessy, dass Ärzte „Gunjah“-Extrakte zur Behandlung einer Vielzahl medizinischer Probleme einsetzten, darunter auch solche, für die es in der westlichen Medizin keine brauchbaren Behandlungen gab. Er studierte die einschlägige Literatur, führte Tierversuche durch und testete die Wirkung von Cannabis an sich selbst, bevor er Patienten behandelte. 1839 stellte O’Shaughnessy seine Erkenntnisse in einem Artikel vor, der in denTransactions of the Medical and Physical Society of Bengal veröffentlicht wurde: „On the Preparations of the Indian Hemp, or Gunjah (Cannabis Indica)“

Dr. Tod Mikuriya hält die erste Ausgabe von O’Shaughnessy’s, das er zusammen mit Fred Gardner gegründet hat.

sensi Star“ ist eine Cannabis afghanica-Sorte mit einem hohen THC-Gehalt.
In einem Krankenhaus in Kalkutta behandelte O’Shaughnessy Patienten mit Rheuma, Hydrophobie, Cholera, Wundstarrkrampf und Epilepsie, „bei denen ein Hanfpräparat eingesetzt wurde, mit Ergebnissen, die es mir rechtfertigen, dass wir uns von seiner umfassenderen und unparteiischen Anwendung eine nicht unerhebliche Bereicherung der ärztlichen Ressourcen versprechen.“
O’Shaughnessys Cannabispräparat – ein Alkoholextrakt – linderte die Symptome aller drei Rheumapatienten in seinem klinischen Versuch. Cannabis rettete den Tetanus-Patienten das Leben (obwohl einer an Wundbrand starb) und ersparte den Hydrophobie-Patienten die schrecklichen Qualen der Tollwut. Bei den Cholera-Patienten linderte es den Durchfall. Und für das kleine Mädchen, das im Alter von 40 Tagen mit „infantilen Krämpfen“ behandelt wurde, berichtete O’Shaughnessy: „Das Kind erfreut sich jetzt einer robusten Gesundheit und hat sein natürliches, pralles und fröhliches Aussehen wiedererlangt.“ O’Shaughnessy war der Meinung, dass indischer Hanf das größte Versprechen als Antikonvulsivum hat.
1841 kehrte O’Shaughnessy nach Großbritannien zurück und brachte seine Botschaft und, was ebenso wichtig war, C. indica-Samen des schmalblättrigen Drogentyps mit. Pflanzen des schmalblättrigen Hanftyps wurden in Großbritannien bereits in großem Umfang zur Fasergewinnung angebaut, aber der schmalblättrige Drogentyp war bis dahin nicht erhältlich. Mit ihrer Ankunft und der Veröffentlichung von O’Shaughnessys Erkenntnissen und Rezepten im Provincial Medical Journal im Jahr 1843 konnten Chemiker starke Tinkturen herstellen, die Ärzte und Patienten nach eigenem Ermessen verwenden konnten. Die westliche Medizin hatte Cannabis für sich entdeckt.
„Die Verwendung von Cannabisderivaten zu medizinischen Zwecken verbreitete sich schnell in der westlichen Medizin“, schrieb Tod Mikuriya, MD, der die frühen Zeitschriftenartikel in Marijuana gesammelt und neu veröffentlicht hat : Medical Papers 1839-1972. Renommierte Ärzte erkannten die Vorteile von Marihuana, darunter William Osler von der Johns Hopkins University, der Cannabis als erste Wahl zur Behandlung von Migräne verschrieb.
In Indien führte die britische Regierung groß angelegte Studien durch, um die „schädlichen Auswirkungen, die angeblich durch den Missbrauch von Ganja hervorgerufen werden“, zu untersuchen Im Jahr 1894 kam einausführlicher Bericht der Indischen Hanf-Drogenkommission zu dem Schluss: „Die allgemeine Meinung scheint zu sein, dass die schädlichen Wirkungen von Ganja übertrieben sind.“
Die Verschreibungen für Medikamente auf Cannabisbasis erreichten in den Vereinigten Staaten zwischen 1890 und 1920 ihren Höhepunkt. Gründe für den sinkenden Marktanteil waren unter anderem die Konkurrenz durch neue und preiswerte synthetische Medikamente wie Aspirin, injizierbare Opiate und Barbiturate sowie die wachsende Verachtung für „rohe“ Kräuter.
Vor allem aber gab es das Problem der uneinheitlichen Potenz. Im U.S. Dispensatory von 1926 heißt es: „Aufgrund der großen Schwankungen in der Potenz verschiedener Cannabisproben ist es nahezu unmöglich, die richtige Dosis einer einzelnen Probe zu bestimmen, es sei denn durch klinische Versuche. Aufgrund gelegentlicher unangenehmer Symptome durch ungewöhnlich starke Präparate sind Ärzte in der Regel mit den verabreichten Mengen übervorsichtig gewesen.“ Mit anderen Worten: Uneinheitliche Potenz führte zu Angst vor Überdosierung, was wiederum zu zu schwachen Cannabispräparaten führte! Das erklärt auch, warum die amerikanischen Verbraucher nicht protestierten, als die Bundesregierung 1937 „Marihuana“ verbot.

Mit Gelatine überzogene Cannabispillen von McKesson & Robbins, einem der vielen US-Drogenunternehmen, die vor dem Verbot 1937 Cannabisextrakte vermarkteten

Reefer Madness ist der Name eines Films, der die Propagandakampagne verkörperte, die 1937 zur Prohibition von Marihuana auf Bundesebene führte.
Die einzige Aussage gegen die Prohibition, als der Kongress darüber debattierte, kam von William Woodward, MD, von der American Medical Association. Woodward argumentierte: „Die medizinische Verwendung von Cannabis hat, wie man Ihnen gesagt hat, enorm abgenommen. Es wird nur noch sehr selten verwendet … teilweise wegen der Ungewissheit über die Wirkung der Droge. Diese Ungewissheit wurde bisher auf Schwankungen in der Potenz der Präparate aus den verwendeten Pflanzen zurückgeführt. Zu sagen, dass der Gebrauch der Droge durch eine Verbotssteuer verhindert werden sollte, wie es hier vorgeschlagen wurde, verkennt jedoch die Tatsache, dass künftige Untersuchungen zeigen könnten, dass es einen wesentlichen medizinischen Nutzen gibt.“ Wie vorausschauend!

Die Pharmakologen Raphael Mechoulam (links) und Yechiel Gaoni ermittelten die genaue Molekularstruktur von THC und CBD und berichteten 1963 und 1964 über ihre Ergebnisse.
1938 beauftragte der Bürgermeister von New York City, Fiorello LaGuardia, die New York Academy of Medicine damit, die Behauptungen zu untersuchen, auf denen das bundesstaatliche Marihuana-Verbot beruhte. Eine hochkarätige Kommission aus Wissenschaftlern und Ärzten kam zu dem Schluss, dass Marihuana nicht süchtig macht und nicht zu Geisteskrankheit und Gewaltverbrechen führt. Exemplare des „LaGuardia Commission Report“ wurden von Agenten des Federal Bureau of Narcotics aufgekauft und vernichtet.
Auf das Ende des Zweiten Weltkriegs folgten fast zwei Jahrzehnte der Dämonisierung von Marihuana und der Menschen, die es konsumierten. Doch Anfang der 1960er Jahre zeigten die Entwicklungen in Wissenschaft und Gesellschaft Risse in der Mauer der Prohibition. Die genauen Molekularstrukturen von THC und CBD wurden 1964 von den israelischen Wissenschaftlern Raphael Mechoulam und Y. Gaoni bestimmt. In diesem Jahr teilte Bob Dylan in New York City Marihuana mit den Beatles und nahm damit eine Ära vorweg, in der Millionen junger Menschen auf der ganzen Welt – vor allem Soldaten und Studenten – Marihuana rauchen, seine Wirkung selbst einschätzen und die Behauptungen der Regierung in Frage stellen würden.

Dr. Mechoulam machte den Begriff „Entourage-Effekt“ populär, um zu beschreiben, wie die Wirkstoffe in Cannabis synergistisch wirken.
Anekdotische Beweise
Diejenigen, die in den 1960er, 70er und 80er Jahren anfingen, Marihuana im sozialen Umfeld zu rauchen, wussten in der Regel nicht, dass es in der nicht allzu fernen Vergangenheit häufig als Medizin verschrieben worden war. Dr. Mikuriya drückte es so aus: „Es war nicht nur Marihuana, das verboten wurde, sondern auch die Wahrheit über die Geschichte
Anekdotische Berichte über die medizinische Wirksamkeit kursierten. Scheinbar kannte jeder jemanden im VA-Krankenhaus, der Marihuana gegen Spastik nahm , oder er hatte eine Tante, die dank des Krauts die Chemotherapie überstand, oder einen Freund, der sagte, dass es ihm beim Schlafen half. Aber weder Ärzte noch Forscher verfolgten die Patienten, die Marihuana konsumierten.
Als Reaktion auf die AIDS-Epidemie gründete 1990 ein Vietnam-Veteran namens Dennis Peron den San Francisco Cannabis Buyers Club. Der Club bot einen Rahmen, in dem Menschen, die Marihuana zu medizinischen Zwecken konsumierten, ihre Erfahrungen austauschen und ein Gefühl für ihre Zahlen bekommen konnten. Mikuriya sah eine „einzigartige Forschungsmöglichkeit“ und begann als medizinischer Koordinator, die Mitglieder zu ihren Krankheiten, ihrem Marihuanakonsum und ihren Ergebnissen zu befragen.
Perons bemerkenswerter Club wurde zum Hauptquartier für Aktivisten, die sich für die Legalisierung von Marihuana zu medizinischen Zwecken einsetzten. Sie entwarfen die „Proposition 215“, eine Gesetzesvorlage, die es Patienten mit ärztlicher Genehmigung erlauben würde, Cannabis zu medizinischen Zwecken zu verwenden. Die kalifornischen Wählerinnen und Wähler haben Prop. 215 im November 1996 mit 56 zu 44 Prozent angenommen – gegen den Widerstand der Strafverfolgungsbehörden und aller gewählten Beamten im Bundesstaat, mit Ausnahme von Terence Hallinan, dem Staatsanwalt von San Francisco.

Dennis Peron vor dem San Francisco Cannabis Buyers Club in der Market Street 1444. 1995 wurde der Club zum Hauptquartier für Aktivisten, die die kalifornische Initiative für medizinisches Marihuana planten.

Beamte der Clinton-Regierung unter der Leitung von Drug Czar Barry McCaffrey prangerten Tod Mikuriya, MD, an und bedrohten Ärzte, die die Verwendung von Marihuana durch ihre Patienten genehmigten, nachdem die kalifornischen Wähler im November 1996 Proposition 215 verabschiedet hatten.
Auf Drängen von Dr. Mikuriya war das neue Gesetz so verfasst worden, dass es nicht nur Patienten mit einigen wenigen schweren Krankheiten, sondern auch solche mit „allen anderen Krankheiten, bei denen Marihuana Linderung verschafft“, erfasst
Im Dezember 1996 drohten der US-Drogenbeauftragte Barry McCaffrey und die Generalstaatsanwältin Janet Reno kalifornischen Ärztinnen und Ärzten, die es wagten, den Marihuana-Konsum von Patienten zu genehmigen, mit dem Entzug ihrer Approbation. Auf einer vielbeachteten Pressekonferenz zeigte McCaffrey spöttisch auf eine große Tabelle mit dem Titel „Dr. Tod Mikuriyas (215 Medical Advisor) Medical Uses of Marijuana“ McCaffrey sagte, es sei völlig absurd, dass ein einziges Medikament bei so vielen Krankheiten wirksam sein könne. „Das ist keine Medizin“, spottete er, „das ist eine Cheech und Chong Show“
Die American Civil Liberties Union und die Reformgruppe, die jetzt als Drug Policy Alliance bekannt ist, unterstützten eine Klage des AIDS-Spezialisten Marcus Conant, MD, um die Regierung daran zu hindern, ihre Drohung wahr zu machen. Die Bundesgerichte stimmten mit den Klägern überein, dass Ärzte und Patienten nach dem ersten Verfassungszusatz das Recht haben, über Marihuana als Behandlungsmöglichkeit zu sprechen.

Cheech und Chong wurden zu Ikonen der Cannabis-Gegenkultur. Ihre Filme und Comedy-Routinen nahmen die angeblichen Gefahren von Marihuana auf die leichte Schulter.
Das Endocannabinoid-System
Während sich der rechtlich-politische Konflikt zuspitzte, gaben Wissenschaftler, die die Wirkung von Cannabis untersuchten, Mikuriya Recht. Im Jahr 1990 – gerade als sich der Cannabis Buyers Club in San Francisco formierte – traf sich eine Gruppe von Wissenschaftlern auf Kreta und gründete die International Cannabis Research Society. Das „C-Wort“ im Namen der Gruppe wurde 1998 in „Cannabinoid“ geändert, weil, wie ein Forscher erklärte, „das Feld sich von der Pflanze wegbewegt“
Die Mitglieder des ICRS waren meist Pharmakologen und Biochemiker, die an akademischen Forschungszentren arbeiteten. Fast alle erhielten oder begehrten Mittel vom US National Institute on Drug Abuse (NIDA), einer Behörde, deren erklärtes Ziel es seit Jahren ist, die Schädlichkeit von Marihuana zu beweisen. Der Heilige Gral der Wissenschaftler war ein Medikament, das die positiven Wirkungen von Cannabis entfaltet, ohne psychoaktiv zu sein.
Auf der Suche nach einem solchen Medikament entdeckten die Forscher das körpereigene Endocannabinoid-Signalsystem – Verbindungen, die im Körper hergestellt werden und körpereigene Rezeptoren aktivieren, die auch auf pflanzliche Cannabinoide reagieren.
Die vorherrschenden Cannabinoide in Cannabispflanzen sind CBD und THC. CBD, das nicht psychoaktiv ist, kommt vor allem in Hanfpflanzen vor, die für Fasern und/oder Samen gezüchtet werden. CBD wurde in den frühen 1940er Jahren von Roger Adams, einem Chemiker der University of Illinois, identifiziert, aber seine genaue Molekularstruktur konnte er nicht herausfinden.
Nach der Entdeckung der Endocannabinoide wurden CBD und THC in „Phytocannabinoide“ umbenannt – Verbindungen, die in der Pflanze vorkommen und fast alle aus 21 Kohlenstoffatomen in Ringstrukturen und Seitenketten bestehen, an denen an verschiedenen Stellen Wasserstoff- und Sauerstoffatome hängen.
Bisher wurden etwa 100 Phytocannabinoide identifiziert, darunter einige biologisch aktive, die ein medizinisches Potenzial haben könnten. (Einige Cannabinoide entstehen flüchtig bei der Analyse des Pflanzenmaterials, andere werden von Enzymen gebildet, die die Pflanzenstoffe verstoffwechseln.)
Zusätzlich zu den Phytocannabinoiden biosynthetisiert die Cannabispflanze Hunderte von chemischen Substanzen, die nicht nur in ihr vorkommen und von denen einige biologisch aktiv sind – darunter Terpene und Flavonoide, die für Geruch, Geschmack und Farbe sorgen. Es wurden drei Flavonoide gefunden, die nur in Cannabis vorkommen: Cannflavin-A, -B und -C.
Endogene („endo-„) Cannabinoide werden in unserem Körper hergestellt, um Signale von einer Nervenzelle zur anderen zu senden. Diese Verbindungen sind in der Tierwelt den pflanzlichen Cannabinoiden in der Reihenfolge ihres evolutionären
auftreten. Endocannabinoide und Phytocannabinoide üben ähnliche Wirkungen aus, wenn sie an Labortieren getestet werden: Verringerung von Schmerzen, Körpertemperatur, spontaner Aktivität und motorischer Kontrolle.
Synthetische Verbindungen, die diese Wirkungen entfalten, werden auch als Cannabinoide bezeichnet. 1974 stellte Eli Lilly Nabilon her, eine synthetische Form von THC, die unter dem Namen Cesamet vermarktet wurde (und Jahre später als Nabilon wieder auf den Markt kam). Mitte der 1980er Jahre produzierte Pfizer eine synthetische Verbindung, CP-55940, die sich als zu psychoaktiv erwies, um als Medikament vermarktet zu werden. Aber im Gegensatz zu THC, das nicht wasserlöslich ist und eine schwache, flüchtige Wirkung hat, kann CP-55940 in wässriger Lösung verarbeitet werden und bindet lange genug, um zu zeigen, wo im Körper es wirkt. Dies war ein großer Segen für die Forschung.
Die Existenz von Cannabinoid-Rezeptoren im Gehirn wurde 1988 von William Devane im Labor von Alynn Howlett an der St. Louis University nachgewiesen. Die Rezeptoren sind Proteine, die in Zellmembranen eingebettet sind. Endocannabinoide oder Phytocannabinoide, die sich an sie binden, lösen eine Kaskade von molekularen Ereignissen in den Zellen aus.
Diese Rezeptoren, die später CB1-Rezeptoren genannt wurden, sind im Kleinhirn und in den Basalganglien konzentriert (Regionen, die für die motorische Kontrolle verantwortlich sind, was erklären könnte, warum Marihuana Berichten zufolge Muskelspastiken lindert), im Hippocampus (Speicherung des Kurzzeitgedächtnisses) und im limbischen System (emotionale Kontrolle). Cannabinoide, die über die CB1-Rezeptoren wirken, spielen eine Rolle bei Belohnungsprozessen, Kognition und Schmerzwahrnehmung sowie bei der motorischen Kontrolle.

sour Tsunami“, gezüchtet von Lawrence Ringo in Humboldt County, ist eine CBD-dominante Sorte. Ringo machte stabilisierte Samen für medizinische Nutzer weithin verfügbar.
1992 wurde ein zweiter Cannabinoid-Rezeptor in den Zellen der Milz, den weißen Blutkörperchen und anderen „peripheren“ Bereichen des Körpers entdeckt. Die Entdeckung des CB2-Rezeptors ließ die Hoffnung aufkeimen, dass wirksame, nicht psychoaktive Medikamente entwickelt werden könnten, die das Immunsystem – und nicht das Gehirn oder das zentrale Nervensystem – beeinflussen.
Ebenfalls 1992 entdeckten Devane und Lumir Hanas, die in Mechoulams Labor an der Hebräischen Universität in Jerusalem arbeiteten, das erste körpereigene Cannabinoid, ein relativ einfaches Molekül namens N-Arachidonylethanolamin (AEA). Sie nannten es „Anandamid“, nach dem Sanskritwort für Glückseligkeit. Anandamid wirkt an den CB1- und CB2-Rezeptoren. Seine Wirkung wird durch THC verdoppelt. Ebenfalls in Mechoulams Labor entdeckte Shimon Ben-Shabat 1994 ein zweites endogenes Cannabinoid, 2-AG (2-Arachidonoylglycerol), das ebenfalls an die CB1- und CB2-Rezeptoren bindet. Im Gegensatz zu Anandamid, das ein relativ schwacher Agonist ist, ist 2-AG im Allgemeinen ein vollständiger Agonist am CB1-Rezeptor.
Anandamid und 2-AG sind ungewöhnliche Neuromodulatoren, da sie über einen Prozess wirken, der „retrograde Signalisierung“ genannt wird Herkömmliche Neurotransmitter – Serotonin, Dopamin usw. – überqueren die Lücke (Synapse) zwischen einer „präsynaptischen“ Sendezelle und einer „postsyaptischen“ Empfangszelle. Endocannabinoide werden bei Bedarf in der postsynaptischen Nervenzelle gebildet und über die Synapse zurückgeschickt, um der sendenden Zelle mitzuteilen, dass sie sich beruhigen oder beschleunigen soll.
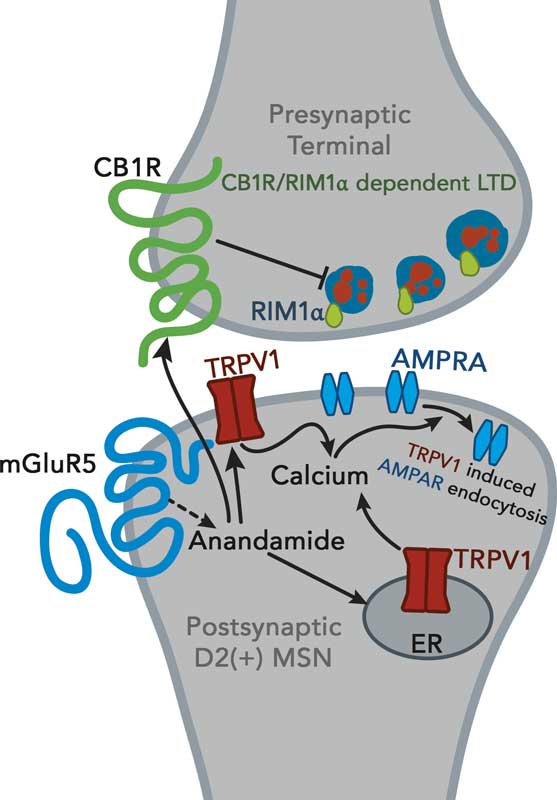
Eine Nervenzelle sendet chemische Signale über einen Spalt – die Synapse – um eine Empfängerzelle zu aktivieren. Endocannabinoide werden aus der Membran der empfangenden Zelle gebildet und über die Synapse zurückgeschickt, um die Geschwindigkeit der Übertragung zu regulieren.
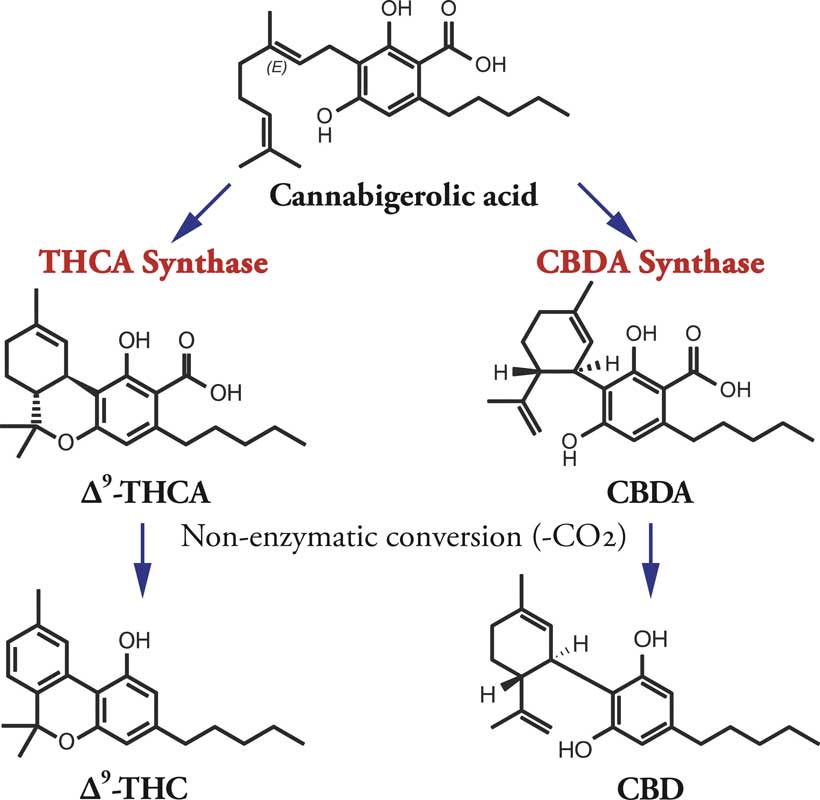
Pflanzliche Cannabinoide haben 21 Kohlenstoffmoleküle, an die an verschiedenen Stellen Sauerstoff und Wasserstoff gebunden sind.
Anandamid und 2-AG stellen das Gleichgewicht – die Homöostase – wieder her, indem sie Nervenzellen, die zu stark feuern, hemmen und Nervenzellen, die zu langsam feuern, enthemmt werden. Stell dir einen Dirigenten vor, der einem Orchester gegenübersteht und das Tempo und die Lautstärke bestimmt, in der die Instrumente ihre Töne erzeugen. Das Endocannabinoid-System ist der
tonangebend im Körper.
Endocannabinoide senden ihre „Bleib-auf-der-Stelle“-Signale in Systeme, die Appetit, Bewegung, Lernen (und Vergessen), Schmerzwahrnehmung, Immunreaktion und Entzündung, Neuroschutz und andere lebenswichtige Prozesse regulieren.
Die Tatsache, dass die Endocannabinoid-Signalübertragung ein wesentlicher Bestandteil jedes physiologischen Prozesses ist, erklärt, warum die Einnahme von Cannabinoiden – z. B. das Inhalieren von Cannabisdampf – Patienten helfen kann, die mit den Symptomen und Krankheiten auf Tod Mikuriyas berüchtigter Liste zu kämpfen haben. Die Wissenschaftler haben erklärt, was er beobachtet und berichtet hat!
Auf der Tagung der International Association for Cannabinoid Medicines im Jahr 2013 zitierte Raphael Mechoulam zustimmend ein Papier, in dem er zu dem Schluss kam, dass „die Modulation der Endocannabinoid-Aktivität bei fast allen Krankheiten, die den Menschen betreffen, ein therapeutisches Potenzial haben kann.“
Bei jedem Jahrestreffen der International Cannabinoid Research Society wurde der Schwerpunkt verstärkt auf therapeutische Anwendungen und weniger auf die Gefahr des Drogenmissbrauchs gelegt. Die Studien, die für das Treffen 2014 eingereicht wurden, spiegeln das erneute Interesse an der Cannabispflanze selbst wider.
Was die Mediziner gelernt haben
Die kalifornische Initiative für medizinisches Marihuana aus dem Jahr 1996 schuf kein Aufzeichnungssystem, weil Dennis Peron und seine Mitautoren keine Masterliste von Cannabiskonsumenten erstellen wollten, die die Staatsanwaltschaft bei Bedarf einsehen könnte. So wurde in all den Jahren seither ein riesiges Experiment im Bereich der öffentlichen Gesundheit durchgeführt, ohne dass irgendeine staatliche Behörde es verfolgte.
Im Jahr 2006, zehn Jahre nach der Legalisierung des medizinischen Konsums, befragte Mikuriya 30 Ärzte, die an den Treffen der California Cannabis Research Medical Group teilgenommen hatten (die er im Jahr 2000 organisiert hatte). Er veröffentlichte die Ergebnisse in O’Shaughnessy’s, einer Zeitschrift, die er 2003 zusammen mit einem von uns (Fred Gardner) gegründet hatte.
Ungefähr 160.000 Patienten hatten von den befragten Ärzten die Erlaubnis erhalten, das Kraut zu verwenden. Die Ärzte waren einhellig beeindruckt von dem Ausmaß, in dem Cannabis es den Patienten ermöglicht, ihre Einnahme von verschreibungspflichtigen und rezeptfreien Medikamenten zu reduzieren. Wie Mikuriya es ausdrückte: „Opioide, Beruhigungsmittel, NSAIDS und SSRI-Antidepressiva werden häufig in geringeren Mengen eingenommen oder abgesetzt. Das sind alles Medikamente mit schwerwiegenden unerwünschten Wirkungen.“
Dr. Robert Sullivan, einer der ersten Ärzte, die in Orange County, Kalifornien, Cannabis-Beratungen anboten, berichtete, dass seine Patienten „Opiate, Muskelrelaxantien, Antidepressiva, Hypnotika (zum Schlafen), Anxiolytika, Neurontin, Entzündungshemmer, Mittel gegen Migräne, Magen-Darm-Medikamente, Prednison (gegen Asthma, Arthritis)“ abgesetzt hatten Cannabis erwies sich als die Anti-Droge.
Berichte über Schmerzpatienten, die Cannabis konsumieren und ihre Opioideinnahme um 50 Prozent reduzieren, passen perfekt zu Studien, die zeigen, dass Labortiere nur halb so viele Opioide benötigen, um eine Schmerzlinderung zu erzielen, wenn sie ebenfalls mit einem Cannabinoid behandelt werden. Ist es da verwunderlich, dass die Hersteller von synthetischen Medikamenten die medizinische Verwendung von Cannabis als Bedrohung für ihre Gewinnmargen ansehen?
Was ist mit den angeblichen schädlichen Wirkungen, einschließlich der Sucht, auf denen das Marihuanaverbot beruht? Dr. Philip Denney sagte über die zehnjährige Studie: „Die Patienten haben so gut wie keine berichtet, abgesehen von den Kontakten mit dem Rechtssystem. Die Patienten können den Cannabiskonsum leicht einstellen, um Drogentests zu bestehen oder auf Reisen zu gehen. Eine Überdosierung von essbarem Cannabis – eine unangenehme Schläfrigkeit, die sechs bis acht Stunden anhält – ist selten und vorübergehend.“
Dr. Frank Lucido antwortete, dass „verminderte Produktivität“ zwei Patienten dazu veranlasste, mit dem Cannabiskonsum aufzuhören. Aber, so fügte er hinzu, „die überwältigende Mehrheit berichtet, dass sie produktiver sind, wenn ihre Symptome mit Cannabis kontrolliert werden.“ Arbeitgeber sollten das beachten.

Die in den Apotheken erhältlichen Cannabisblüten haben es den Patienten in den Staaten mit medizinischem Marihuana ermöglicht, die Einnahme von synthetischen Medikamenten, die unerwünschte Nebenwirkungen haben, zu reduzieren oder ganz einzustellen.
Die CBD-Ära
Die Verabschiedung der Proposition 215 in Kalifornien ermutigte Menschen auf der ganzen Welt, sich für den Zugang zu medizinischem Cannabis einzusetzen. Multiple Sklerose (MS)-Patienten in England begannen, das Gesundheitsministerium mit zunehmender Dringlichkeit zu beeinflussen. Im Frühjahr 1997 hielten MS-Patienten eine öffentliche Versammlung in London ab, die die Aufmerksamkeit des pharmazeutischen Unternehmers Geoffrey Guy, MD, auf sich zog, der versprach, sie bei der Erreichung ihres Ziels zu unterstützen.
Guy stellte fest, dass Cannabis, das in England von MS-Patienten und anderen, die über medizinische Vorteile berichteten, verwendet wurde, neben THC auch erhebliche Mengen an CBD enthielt. Die geringere Psychoaktivität von CBD-reichem Cannabis sollte ein wichtiges Verkaufsargument sein, als er dem Innenministerium seinen Plan vorstellte, ein Cannabismedikament in pharmazeutischer Qualität herzustellen. Sein Unternehmen GW Pharmaceuticals erhielt im Frühjahr 1998 die Genehmigung, Cannabis zu diesem Zweck anzubauen.
Um eine Marktzulassung zu erhalten, mussten die Extrakte von GW mit nahezu perfekter Konsistenz hergestellt werden und in klinischen Versuchen ihre Sicherheit und Wirksamkeit beweisen. Guys erster Schritt war der Kauf der genetisch vielfältigen Pflanzensammlung von Hortapharm, einer niederländischen Firma, die in den 1980er Jahren von den amerikanischen Ex-Pats David Watson und Robert Clarke gegründet wurde.
Sie waren es, die erkannten, dass CBD und andere Verbindungen als THC erhebliche Wirkungen haben. Sie reisten um den Globus und sammelten „Landrassen“-Sorten, von denen einige erhebliche Mengen dieser bis dahin unbeachteten „kleinen“ Cannabinoide enthielten Watson und Clarke erkannten auch, dass die Terpenoide, die den Cannabissorten ihr Aroma verleihen, bei der Einnahme eine Wirkung entfalten.
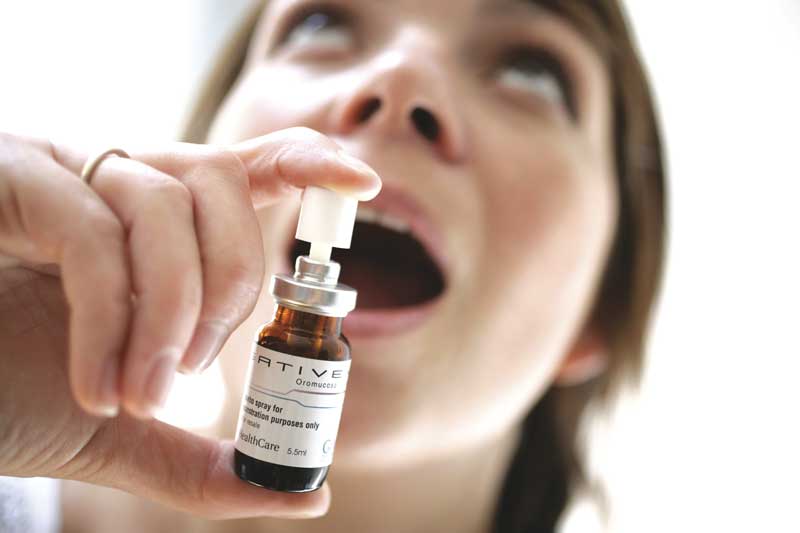
Sativex von GW Pharmaceuticals, ein sublinguales Cannabinoidspray, besteht aus ungefähr gleichen Mengen CBD und THC.
GW begann mit dem Anbau von Tausenden von Pflanzen in hochmodernen Gewächshäusern im Südosten Englands. Neben der Entwicklung von Sorten mit hohem THC- und CBD-Gehalt züchtete GW auch Pflanzen mit einem hohen Gehalt an Cannabichromen (CBC), Cannabigerol (CBG) und Tetrahydrocannabivarin (THCV), um deren medizinische Wirkung zu testen. In den letzten Jahren wurde Cannabidivarin (CBDV) zu einem für das Unternehmen interessanten Wirkstoff.
1999 stellte GW sein Flaggschiff, Sativex, her – einen Extrakt aus der ganzen Pflanze, der unter die Zunge gesprüht werden kann. Sativex enthält ungefähr gleiche Mengen an CBD und THC sowie Spuren aller anderen von der Pflanze produzierten Verbindungen. GW initiierte klinische Versuche und begann, Sativex und andere Cannabisextrakte an Forscher zu liefern. Ihre Ergebnisse, über die in den folgenden Jahren in Zeitschriftenartikeln und auf Konferenzen berichtet wurde, legen nahe, dass CBD die Symptome von rheumatoider Arthritis, Diabetes, Epilepsie, Alkoholismus, PTBS, antibiotikaresistenten Infektionen und neurologischen Störungen lindern kann. CBD zeigte auch neuroprotektive und krebshemmende Wirkungen. Menschen, die Sativex verwenden, nehmen weniger Opiate und andere Medikamente ein. Sativex hatte weniger und mildere Nebenwirkungen als reines THC (Marinol).
Im April 2005 erhielt Sativex von Health Canada eine bedingte Zulassung zur Behandlung von Schmerzen bei MS. Das Vereinigte Königreich und etwa 20 weitere Länder haben Sativex zur Behandlung von Spastizität bei MS zugelassen. In den USA und anderen Ländern wird Sativex derzeit in klinischen Studien zur Behandlung von Krebsschmerzen getestet.
Viele Jahre lang ging man davon aus, dass der CBD-Gehalt in allen Cannabispflanzen , die in den USA für medizinische und Freizeitzwecke angebaut werden, bis auf Spuren heruntergezüchtet worden war. Da keine chemischen Analyselabore Cannabisproben untersuchten, gab es keine Möglichkeit, den Cannabinoidgehalt zu bestimmen. Diese Situation änderte sich im Winter 2008-2009, als Steve DeAngelo, Leiter des Harborside Health Center in Oakland, zwei ehemalige Anbauer, David Lampach und Addison DeMoura, dazu ermutigte, ein Labor mit dem treffenden Namen Steep Hill zu gründen.
Harborside belieferte das Labor mit einem ständigen Strom von Proben, die auf Schimmelpilzbefall und auf den Gehalt an THC, CBD und CBN untersucht wurden.
Es stellte sich heraus, dass CBD-reiches Cannabis in Kalifornien gar nicht so selten war, wie Experten vorhergesagt hatten. O’Shaughnessy’s berichtete, dass etwa eine von 600 Proben, die 2009 zu Steep Hill und anderen Laboren gebracht wurden, 4 Prozent oder mehr CBD enthielt. ProjectCBD wurde ins Leben gerufen, um darüber zu berichten, was Ärzte, Patienten, Anbauer und Hersteller über CBD-reiche Medikamente erfahren.
P.S. (Post Sanjay)
Im August 2013 sprach Dr. Sanjay Gupta in einer CNN-Dokumentation, in der er einräumte, dass wir alle über Marihuana „systematisch fehlgebildet“ wurden. In der Sendung wurden dramatische Beispiele für die positive Wirkung von Cannabis gezeigt. Am einprägsamsten war die Geschichte der fünfjährigen Charlotte Figi, die an einer schweren Form von Epilepsie litt.
Charlottes Anfälle hatten sich verschlimmert, als herkömmliche Behandlungen versagten. Ihre Mutter in Colorado Springs und ihr Vater, ein Unteroffizier der Special Forces, der in Afghanistan stationiert ist, recherchierten im Internet und erfuhren von Cannabis als Antikonvulsivum. Paige Figi besorgte sich Knospen von Apotheken und ein Freund brachte ihr bei, wie man Öl für Charlotte gewinnt. Eine CBD-reiche Sorte wirkte anfallslindernd, aber Paige konnte sich nicht mit Nachschub versorgen.

Wernard Bruining gründete 1972 den ersten Coffee Shop in Amsterdam, Mellow Yellow. Heute ist er die niederländische Avantgarde für medizinisches Cannabis. Auf seiner Website www.mediwiet.nl findest du weitere Informationen.
Foto von Lika Bruining.

Dr. Sanjay Gupta und Geoffrey Guy in der Anbaufabrik von GW Pharmaceuticals. GW bemüht sich um die FDA-Zulassung für Sativex (zur Behandlung von hartnäckigen Krebsschmerzen) und Epidiolex (für pädiatrische Epilepsien).
Im Februar 2012 lernte sie Joel Stanley kennen, der mit seinen Brüdern Marihuana für ihre eigenen Apotheken anbaute und eine Hanfsorte besaß, die bei Charlotte auf wundersame Weise gut funktionierte. Die Stanleys nannten ihre Pflanze „Charlotte’s Web“ und boten an, sie in großen Mengen für die Figis und andere Bedürftige anzubauen. Als Sanjay Gupta ihr Gewächshaus besuchte, zeigte einer der Stanleys-Brüder auf eine Charlotte’s Web-Pflanze und behauptete: „So etwas gibt es auf der Welt nicht. Diese Pflanze hat 21 Prozent CBD und weniger als 1 Prozent THC.“
Glücklicherweise gibt es andere Cannabispflanzen mit einem CBD:THC-Verhältnis von mehr als 20:1, die in Kalifornien und anderen Staaten, in denen dies legal ist, angebaut werden. Es ist auch nicht klar, dass die Medizin umso wirksamer ist, je höher das Verhältnis von CBD zu THC ist. Vielleicht gibt es ein optimales Verhältnis für die Behandlung jeder Krankheit und jedes Einzelnen. Der Gehalt an Terpenoiden und Flavonoiden beeinflusst die Wirkung von Medikamenten, die auf Cannabis basieren. Für Ärztinnen und Ärzte, Patientinnen und Patienten, Anbauerinnen und Anbauer sowie Herstellerinnen und Hersteller von Medikamenten bietet sich eine herausfordernde Forschungsmöglichkeit.
Das Bundesgesetz über die Landwirtschaft von 2014 hat den Anbau von „Industriehanf“ mit einem THC-Gehalt von 0,3 Prozent oder weniger zu Forschungszwecken legalisiert. Dies ermöglichte es den Stanley Brothers, auf 17 Hektar 36.000 Charlotte’s Web-Pflanzen anzubauen, die jetzt einen CBD-THC-Gehalt von 30:1 aufweisen, und ihren Extrakt als CW Hanföl zu bezeichnen. Auch in Kentucky wurden mehrere tausend Hanfpflanzen für medizinische Zwecke angebaut. „Industriehanf“ liefert mehr als nur Nahrungsmittel und Fasern. Im Kongress wurde ein Gesetzesentwurf eingebracht, der CBD und Hanf aus dem Controlled Substances Act streichen soll.
Hunderte von Eltern von Kindern mit Epilepsie, Krebs und anderen schweren Krankheiten sind nach Colorado gezogen, in der Hoffnung, Charlotte’s Web zu bekommen. Die gemeinnützige Organisation Realm of Caring, die von Paige Figi mitbegründet wurde, berät Familien, die das Produkt der Gebrüder Stanley verwenden, führt eine Warteliste mit potenziellen Kunden und dient als Informationsquelle. Im Jahr 2014 haben elf Staaten Gesetze verabschiedet, die Cannabis mit geringen Mengen an THC legalisieren. Verbotsbefürworter sind der Meinung, dass diese so genannten CBD-Gesetze die Unterstützung von Gesetzen abziehen, die THC für medizinische Zwecke legalisieren würden (wie im November 2014 in Florida geschehen). Befürworter sehen sie als einen ersten Schritt zu einer umfassenderen Gesetzgebung.
Zahlreiche Unternehmen produzieren und vertreiben Medikamente auf Cannabisbasis in den USA und in Übersee. Die dreistesten verkaufen CBD-haltige Produkte über den Postweg und online. Obwohl CBD weiterhin auf Liste Eins des Bundesgesetzes über kontrollierte Substanzen steht, sind Hanfprodukte mit weniger als 0,3 Prozent THC legal (und bei Costco erhältlich).

Lawrence Ringo (links) und Jaime Carion („Cannatonic“-Züchter, Resin Seeds) auf dem High Times Medical Cannabis Cup in San Francisco. Niemand hat mehr dazu beigetragen, die Verfügbarkeit von CBD-reichen Pflanzen für medizinische Zwecke zu beschleunigen und auszuweiten, als diese beiden Männer.
Die Bundesbehörden sind nicht gegen Unternehmen vorgegangen, die medizinische Produkte importieren, die größere Mengen CBD enthalten, das aus legal in Übersee angebauten Hanfpflanzen gewonnen wird. Die Gebrüder Stanley – denen 2014 davon abgeraten wurde, Charlotte’s Web Hanföl aus Colorado an Patienten in anderen Bundesstaaten zu verschicken – planen nun, Pflanzen in Uruguay und anderen Ländern anzubauen und das Öl an Patienten in den USA zu verschicken.
GW Pharmaceuticals beantragt die FDA-Zulassung für Epidiolex, ein CBD-Extrakt ohne THC. Epidiolex wurde 2014 Epilepsiespezialisten zur Verfügung gestellt, die an Krankenhäusern in den USA ein IND-Programm (Investigational New Drug) mit rund 200 Kindern durchführten. Bei mehr als der Hälfte der Kinder traten deutlich weniger und weniger schwere Anfälle auf. Etwa 15 Prozent blieben anfallsfrei und etwa 15 Prozent wurden anfallsfrei. Ein ähnliches Muster wurde von den Ärzten Bonni Goldstein, MD, und Margaret Gedde, MD, berichtet, die in Los Angeles bzw. Colorado Springs Hunderte von Kindern mit CBD-reichem Cannabis gegen Epilepsie behandeln.
Martin Lee, Organisator von Project CBD, sagt: „Welch eine Ironie, dass das Cannabisverbot, das dem Kongress und der leichtgläubigen Öffentlichkeit als Mittel zum Schutz der Kinder vor einem tödlichen Laster präsentiert wurde, nun bröckelt, weil die Kinder Cannabis als Medizin dringend brauchen.“
Die von Tod Mikuriya im Jahr 2000 gegründete Ärztegruppe, die heute als Society of Cannabis Clinicians bekannt ist, hatte im Juni 2014 mehr als 100 Mitglieder. Die SCC wird seit 2009 von Jeffrey Hergenrather, MD, einem der Gründungsmitglieder, geleitet. „Das Verständnis von Ärzten und Patienten für die Wirkungsweise von Cannabis hat sich in den letzten Jahren deutlich verbessert“, sagt er. „Jetzt ist es an der Zeit, dass die medizinischen Fakultäten das Endocannabinoid-System anerkennen.“
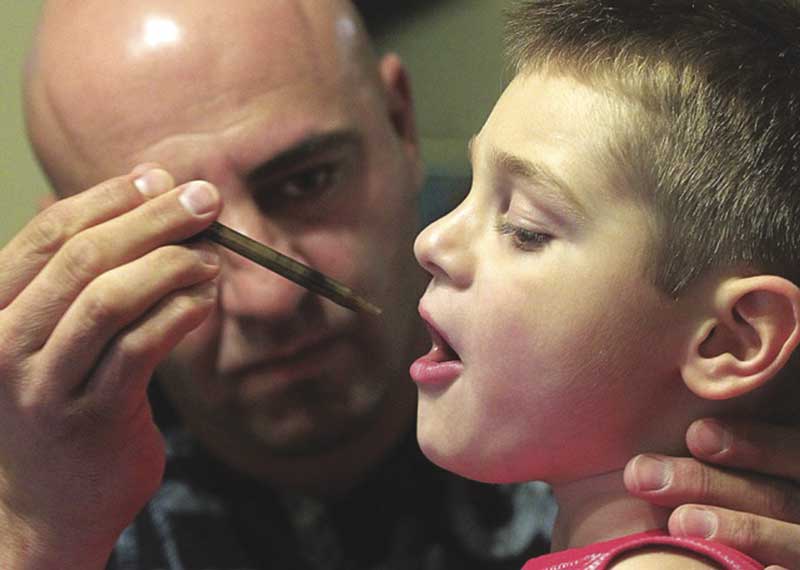
Jason David suministró aceite rico en CBD del Harborside Health Center de Oakland a su hijo Jayden, que consiguió aliviar las convulsiones. La noticia de la mejoría de Jayden inspiró a los padres de Charlotte Figi a buscar CBD en Colorado. Foto de Braverman Productions.
Interessante Links
O’Shaughnessy’s, berichtet über die Geschichte der medizinischen Marihuana-Bewegung.
ProjectCBD.org berichtet über die Verfügbarkeit von CBD und darüber, was Wissenschaftler, Ärzte, Patienten und Anbauer darüber lernen.
Die CBD Crew, eine Partnerschaft zwischen Mr. Nice und Resin Seeds, produziert CBD-reiche Sorten.

