por Fred Gardner e Dr. John McPartland.
Só podemos imaginar como é que as pessoas, há inúmeros milhares de anos, descobriram que uma determinada planta tinha propriedades curativas. Talvez uma mulher estivesse a colher sementes para se alimentar quando começou um período doloroso. Quando tirava as sementes das flores da planta, uma resina pegajosa cobria-lhe as mãos. Roeu um pouco da substância pegajosa. Pouco tempo depois, começou a sentir-se melhor.
Os seus amigos confirmaram que se tratava, de facto, de uma planta que reduzia as cãibras. Começaram a cultivá-la de propósito. Quando a sua tribo se mudou, trouxeram sementes para plantar na povoação seguinte. Descobertas semelhantes devem ter sido feitas muitas vezes em muitos grupos. As pessoas aperceberam-se de que as sementes eram nutritivas, a resina era analgésica e o caule fornecia fibras para cordas e redes.
Aqui e ali, as tribos começaram a cultivar intencionalmente esta planta especialmente útil. Os pormenores perderam-se nas brumas da história, mas a planta permanece e é agora conhecida pelos botânicos como Cannabis. (O nome latino da planta está em itálico, mas cannabis, o produto feito a partir da planta, não está)
A Cannabis evoluiu muito antes dos humanos, mas como ninguém encontrou macrofósseis de Cannabis em rochas, é difícil dizer quando. Dois estudos de ADN estimam que a Cannabis evoluiu há 21 ou 27,8 milhões de anos. O pólen fossilizado identificado como Cannabis data de há 787.000 anos no sul da Sibéria.
Pólen mais jovem, com cerca de 125.000 anos, foi extraído de um pântano da Sibéria. Ossos de Neanderthal da mesma data foram encontrados numa caverna a 30 milhas de distância. Algum tempo depois de o Homo sapiens ter migrado para a região, há 40.000 anos, estabelecemos uma parceria com a planta.
“O cânhamo seguiu o homem naturalmente”, escreveu Nicolai Vavilov, o grande cientista vegetal russo, “mantendo-se perto das suas habitações, instalando-se no lixo e em todos os lugares onde o solo era adubado” A imagem de “seguidor do campo” do cânhamo foi popularizada por Edgar Anderson, um conhecido botânico da Universidade de Harvard e do Jardim Botânico do Missouri.
A certa altura, as pessoas começaram a selecionar as plantas com as características que apreciavam para cultivo – caules altos, sementes grandes e oleosas ou resina psicoactiva e curativa. Vavilov, Anderson, Carl Sauer, Andrew Sherratt e Carl Sagan relacionaram as origens da agricultura com os esforços dos nossos antepassados para cultivar Cannabis mais útil. Sauer propôs que a agricultura foi desenvolvida por pessoas que viviam em comunidades piscatórias junto a rios e lagos (o habitat da “ditchweed”) e que começaram a cultivar as plantas como fonte de linhas e redes de pesca. Ninguém sabe exatamente onde e quando.

Cultivo de canábis nas montanhas Rif, em Marrocos
Classificação
O botânico sueco Carl Linnaeus descreveu formalmente a Cannabis sativa em 1753. Trinta e dois anos mais tarde, Jean Baptiste Lamarck identificou a Cannabis indica como uma segunda espécie. Os especialistas continuam a debater se devem ser classificadas como espécies separadas ou como variedades separadas de uma espécie. As populações existentes de uma possível terceira espécie, a Cannabis ruderalis, podem ser uma relíquia de tipo selvagem que descende do antepassado da C. sativa.
Depois veio o That ’70s Show, quando a taxonomia da canábis se envolveu no sistema legal dos EUA. O etnobotânico Richard Evans Schultes, uma testemunha de defesa, afirmou que as leis sobre narcóticos se referiam à C. sativa, enquanto o arguido possuía C. indica, que era ignorada por lei e tecnicamente legal. Ernest Small, um botânico taxonómico, defendeu a existência de uma única espécie em nome dos queixosos.
Infelizmente, Schultes e o seu colega Loren Anderson fizeram alterações subtis na taxonomia da canábis que se afastaram dos conceitos originais de Linnaeus e Lamarck. Incluíram plantas de droga e plantas de fibra na C. sativa. (Sabemos agora que as plantas de droga são ricas em 9-tetrahidrocanabinol ou THC, e as plantas do tipo fibra são ricas em canabidiol ou CBD) Os espécimes de C. sativa de Linnaeus foram examinados por William Stern em 1974 e foram considerados “antigas variedades de cânhamo cultivadas no norte da Europa” – plantas dominantes de cânhamo, não de droga – com CBD.

David Bronner, conservacionista e ativista do cânhamo, presidente da Dr. Bronner’s Magic Soaps, inspecciona um campo de cânhamo industrial no Colorado, 2013. Para mais informações, consulta www.drbronner.com.
Schultes e Anderson delimitaram a C. indica às plantas que Schultes viu no Afeganistão. Assim, caracterizaram a “indica” como plantas curtas, densamente ramificadas e com folhetos largos, e a “sativa” de acordo com as espécies de Lamarck – altas, pouco ramificadas e com folhetos estreitos. Estas duas espécies deram origem à taxonomia vernacular de “sativa” e “indica” que ainda hoje é utilizada. Com o interesse crescente em plantas com alto teor de CBD, algumas das quais são C. sativa no sentido de Linnaean, a taxonomia vernacular tornou-se verdadeiramente confusa.
O botânico Karl Hillig separa estas populações: A C. sativa representa as plantas com predominância de CBD da Europa, quer cultivadas( biótipo de cânhamo daC. sativa ) quer de tipo selvagem( biótipo feral daC. sativa ).
AC. indica representa as plantas asiáticas com predominância de THC, quer as plantas de Lamarck da Índia – C. indica NLD (“narrow leaflet diameter”, conhecido como “sativa” no vernáculo), quer as plantas do Afeganistão – C. indica WLD (“wild leaflet diameter”, o vernáculo “indica”).
Os naturalistas Robert Clarke e Mark Merlin adoptaram o sistema de Hillig e expandiram-no. Examinando a distribuição mundial das plantas de Cannabis – selvagens, cultivadas e ferozes (uma vez cultivadas, novamente selvagens) – estes especialistas concluem que:
O cânhamo de folha estreita, C. sativa, subespécie sativa, foi cultivado predominantemente na Europa.
O cânhamo de folha larga, C. indica, subespécie chinensis, foi cultivado na China, Coreia, Japão e Sudeste Asiático.
As plantas estupefacientes de folha estreita, C. indica, subespécie indica, eram cultivadas no Sul e Sudeste Asiático e no Médio Oriente.
As plantas medicinais de folha larga, C. indica, subespécie afghanica, foram cultivadas no Norte do Afeganistão e no Paquistão.
Nota que o cruzamento e a hibridação generalizada de plantas de folha estreita e de folha larga tornou a aplicação destes termos botanicamente imprecisa em muitos casos.
Uso medicinal antes da era moderna
Todos os famosos berços da civilização do Velho Mundo utilizaram a canábis para fins medicinais – China, Mesopotâmia, Grécia, Índia e talvez Egipto. Os citas, uma tribo de migrantes que inalavam vapor de canábis para fins rituais, saíram da sua terra natal na Sibéria por volta de 800 AC. Não tinham uma língua escrita, mas a sua palavra para Cannabis foi reconstruída como kanab, kanap, konaba, ou kannabis. Os citas influenciaram as civilizações da China, Índia e Mesopotâmia no início da história.
O médico e historiador Ethan Russo visitou um túmulo no cemitério de Yánghai que continha quase um quilo de canábis. Era uma planta rudimentar – copas floridas, folhas e sementes, sem caules. A sepultura não continha fibras de cânhamo. Data de 766-416 a.C. Os citas estão enterrados nas proximidades. Yánghai situa-se na bacia de Turpan, atualmente parte da China.
Os antigos chineses conheciam a canábis como “má” O seu pictograma para má representa duas plantas penduradas de cabeça para baixo para secar. A combinação de má com o carácter yào (droga) significa “narcótico” ou “anestésico”
O lendário médico Shénnóng escreve extensivamente sobre má no seu texto médico de sabor tauista, Shénnóng Ben Cao Jing (também conhecido como Pen Ts’ao Ching). Avisa: “Tomar muito pode fazer com que vejas fantasmas e corras freneticamente. Se o tomares durante muito tempo, poderás comunicar com o espírito e tornar o corpo leve” Shénnóng terá vivido há cerca de 4000 anos, mas a sua lendária existência não foi mencionada até cerca de 130 a.C.
Os citas entraram na história quando invadiram a Mesopotâmia durante o reinado do rei Sargão II (722 705 a.C.). Depois de os citas terem invadido a Assíria, surgiu uma nova palavra no cuneiforme neo-assírio. A palavra, que significa “cânhamo”, translitera-se como qunubu ou qunnabu. A palavra aparece em contextos que sugerem a sua utilização por xamãs, o que reforça a ligação cita.

O pictograma chinês “má” representa a canábis – duas plantas penduradas de cabeça para baixo para secar.

A divindade hindu Shiva há muito que é associada à canábis.
Heródoto, o “pai da história” grego, escreveu extensivamente sobre os citas por volta de 440 a.C. Heródoto cunhou a palavra xávvaßiç a partir de uma palavra que adoptou dos citas . Descreve-os a usar xávvaßiç para cordas e tecidos e a vaporizar xávvaßiç em pequenas tendas.
Na Índia existem mais de 50 palavras para designar a canábis e os seus produtos. Arqueólogos que trabalham na bacia do rio Ganges descobriram sementes de canábis de pelo menos 1300 a.C. O Atharvaveda, compilado por volta de 900 a.C., dá o nome bhånga a uma planta que muitos especialistas acreditam ser Cannabis. Estas datas precedem a chegada dos citas, cuja presença mais antiga no Hindu Kush pode datar do século VII a.C.
Siddhartha Gautama (ca. 563-483 a.C.), o Buda da nossa era histórica, era um indo-cita. Supostamente, alimentava-se de uma semente de cânhamo por dia durante os seus seis passos de ascetismo. Os praticantes da medicina ayurvédica, o sistema tradicional indiano, recomendam a erva para combater a dor, a insónia e a perda de apetite.
O hieróglifo egípcio šmšmt foi interpretado como Cannabis. A palavra aparece nos Textos das Pirâmides de 2350 a.C., “os cordões (ou cordas) da planta šmšmt ” No entanto, o linho e não o cânhamo era a principal cultura de fibras do antigo Egipto. Outros autores interpretam šmšmt como Corchorus olitorius, uma erva fibrosa cujas folhas são comidas e usadas medicinalmente no Egipto. A palavra também se assemelha a šmšm, a palavra árabe para sésamo. As boas provas da canábis no Egipto começam na era romana.
A notável antropóloga polaca Sara Benet (neé Benetowa) argumenta que kaneh bosm (qaneh bosem) é Cannabis no Antigo Testamento, Êxodo 30:22-25. A palavra é geralmente traduzida como “cana aromática” Moisés usou kaneh bosm para um óleo de unção sagrado. Benetowa nota “a surpreendente semelhança” entre kanbos semítico e a palavra cita para Cannabis. Mas o Livro do Êxodo foi composto por volta do século VIII ou IX a.C., e os citas só invadiram a Terra de Israel em 630 a.C. Nessa altura, os israelitas já tinham sido dispersos e exilados pelos assírios.
A canábis não é originária do Crescente Fértil. Kanbos, que também se translitera kanbus ou qannabbôs, aparece pela primeira vez na Mishnah, escrita no século I a.C.
Dada a evidência de que os produtos de canábis eram amplamente utilizados para tratar doenças no mundo antigo, o verdadeiro mistério é porque é que caiu em desuso – um fenómeno histórico que Ethan Russo apelidou de “Cannabis interruptus” Procurando uma explicação, Russo citou “a natureza perecível” do registo histórico e “a propensão da humanidade para guerras constantes, invasões e conflitos culturais”
É como se os proibicionistas sempre tivessem existido em todas as sociedades e, de tempos a tempos, prevalecessem sobre os médicos e os doentes que deram bom uso aos produtos de canábis. Uma teoria é que, em muitas culturas, os membros da classe sacerdotal viam as plantas psicoactivas como uma ameaça ao seu papel de intermediários adequados entre os reinos material e espiritual. Não queriam que as pessoas tivessem visões e ideias criativas sem a sua supervisão. Nos tempos modernos, a proibição da cannabis constituiu um método eficaz de controlo social – um mecanismo para financiar e armar a polícia e um marcador de desobediência entre os cidadãos.
O padrão de a canábis se revelar medicamente útil, mas ser proibida, continuou em várias partes do mundo durante a Idade Média. No Egipto islâmico, de acordo com Russo, “enquanto muitos ridicularizavam os seus efeitos psicoactivos com base na proibição de intoxicantes prevista na sharia muçulmana, era frequente o reconhecimento a contragosto dos seus abundantes atributos medicinais”
Um rei egípcio impôs uma proibição no século XIII, mas quando Napoleão invadiu o Egipto em 1798, o uso da erva estava generalizado e os franceses acharam por bem impor a sua própria proibição. Trinta anos mais tarde, um médico francês, Aubert-Roche, relatou que durante um surto de peste em Alexandria, a canábis aliviou a febre, a agitação, a dor, a bronquite e a insónia. E assim o pêndulo continuou a oscilar entre a proscrição e a prescrição.
A canábis na literatura médica
A Inglaterra, tal como a França, descobriu a canábis medicinal através das suas colónias. A notícia foi dada por um brilhante médico nascido na Irlanda e educado em Edimburgo, chamado William Brooke O’Shaughnessy. A Companhia Britânica das Índias Orientais enviou O’Shaughnessy para Calcutá na década de 1830. Era uma jovem estrela, tendo já recebido elogios por ter concebido um tratamento eficaz para a cólera – a terapia de substituição electrolítica – que viria a dar origem à administração intravenosa de medicamentos.
Na Índia, O’Shaughnessy observou que os médicos estavam a utilizar extractos de “gunjah” para tratar uma vasta gama de problemas médicos, incluindo alguns para os quais a medicina ocidental não tinha tratamentos úteis. Estudou a literatura relevante, realizou estudos em animais e testou os efeitos da canábis em si próprio antes de tratar os pacientes. Em 1839, O’Shaughnessy apresentou as suas descobertas num artigo publicado nasTransacções da Sociedade Médica e Física de Bengala: “Sobre as Preparações do Cânhamo Indiano, ou Gunjah (Cannabis Indica)”

O Dr. Tod Mikuriya segura a primeira edição da O’Shaughnessy’s, que co-fundou com Fred Gardner.

a ‘Sensi Star’ é uma variedade da Cannabis afghanica com um elevado teor de THC.
Num hospital em Calcutá, O’Shaughnessy tratou pacientes com reumatismo, hidrofobia, cólera, tétano e epilepsia, “nos quais foi utilizada uma preparação de cânhamo com resultados que me parecem justificar a antecipação de uma utilização mais extensa e imparcial, sem que isso represente um acréscimo considerável aos recursos do médico”
O preparado de canábis de O’Shaughnessy – um extrato de álcool – aliviou os sintomas dos três doentes de reumatismo no seu ensaio clínico. A canábis salvou a vida dos doentes com tétano (embora um tenha morrido de gangrena) e poupou os doentes com hidrofobia às terríveis agonias associadas à raiva. Reduziu a diarreia nos doentes com cólera. E quanto à menina que foi observada aos 40 dias com “convulsão infantil”, O’Shaughnessy relatou: “A criança está agora a gozar de uma saúde robusta e recuperou a sua aparência natural, rechonchuda e feliz.” O’Shaughnessy achava que o cânhamo indiano era o mais promissor como anticonvulsivo.
Em 1841, O’Shaughnessy regressou à Grã-Bretanha com a sua mensagem e, igualmente importante, com sementes de C. indica do tipo droga de folha estreita. As plantas do tipo cânhamo de folha estreita tinham sido amplamente cultivadas para a produção de fibras na Grã-Bretanha, mas o tipo droga de folha estreita não estava até então disponível. A sua chegada e a publicação, em 1843, das descobertas e receitas de O’Shaughnessy no Provincial Medical Journal permitiram aos químicos produzir tinturas potentes para utilização por médicos e pacientes. A medicina ocidental tinha passado a utilizar a canábis.
“A utilização de derivados de canábis para fins medicinais espalhou-se rapidamente por toda a medicina ocidental”, escreveu Tod Mikuriya, médico, que recolheu e republicou os primeiros artigos de jornais em Marijuana: Medical Papers 1839-1972. Médicos de prestígio notaram os seus benefícios, incluindo William Osler, da Universidade Johns Hopkins, que prescreveu a canábis como tratamento de primeira linha para enxaquecas.
Na Índia, o governo britânico levou a cabo estudos em grande escala para investigar os “efeitos deletérios alegadamente produzidos pelo abuso da ganja” Em 1894, umrelatório exaustivo da Comissão Indiana de Drogas de Cânhamo concluiu: “A opinião geral parece ser a de que os efeitos nocivos da ganja foram exagerados.”
As prescrições de medicamentos à base de canábis atingiram um pico entre 1890 e 1920 nos Estados Unidos. Os factores que contribuíram para o declínio da quota de mercado foram a concorrência de medicamentos sintéticos novos e baratos, como a aspirina, os opiáceos injectáveis e os barbitúricos, e um desdém crescente pelas ervas “brutas”.
Acima de tudo, havia o problema da potência inconsistente. Como explica o Dispensatório dos EUA de 1926, “devido à grande variabilidade na potência de diferentes amostras de canábis, é praticamente impossível determinar a dose adequada de qualquer amostra individual, exceto através de ensaios clínicos. Devido a sintomas desagradáveis ocasionais provocados por preparações invulgarmente potentes, os médicos têm sido geralmente demasiado cautelosos nas quantidades administradas.” Por outras palavras, a potência inconsistente levou ao medo de overdose, o que levou a preparações de canábis demasiado fracas! Isto ajuda a explicar porque é que os consumidores americanos não protestaram quando o governo federal proibiu a “marijuana” em 1937.

Comprimidos de canábis revestidos de gelatina produzidos pela McKesson & Robbins, uma das muitas empresas farmacêuticas americanas que comercializavam extractos de canábis antes da proibição em 1937

Reefer Madness é o nome de um filme que veio a simbolizar a campanha de propaganda que levou à proibição federal da marijuana em 1937.
O único testemunho contra a proibição quando o Congresso a debateu veio de William Woodward, médico da Associação Médica Americana. Woodward argumentou: “O uso medicinal da Cannabis, como te foi dito, diminuiu enormemente. É muito raramente utilizada… em parte devido à incerteza dos efeitos da droga. Essa incerteza foi até agora atribuída a variações na potência das preparações provenientes de plantas específicas utilizadas… Dizer, no entanto, como foi aqui proposto, que o uso da droga deve ser impedido por um imposto proibitivo, perde de vista o facto de que a investigação futura pode mostrar que existem usos médicos substanciais.” Que presciente!

Os farmacologistas Raphael Mechoulam (à esquerda) e Yechiel Gaoni descobriram a estrutura molecular exacta do THC e do CBD e comunicaram as suas descobertas em 1963 e 1964.
Em 1938, o Presidente da Câmara de Nova Iorque, Fiorello LaGuardia, designou a Academia de Medicina de Nova Iorque para investigar as alegações em que se baseava a proibição federal da marijuana. Uma comissão de cientistas e médicos concluiu que a marijuana não causa dependência e não conduz à insanidade e a crimes violentos. Cópias do “Relatório da Comissão LaGuardia” foram compradas e destruídas por agentes do Departamento Federal de Narcóticos.
O fim da Segunda Guerra Mundial foi seguido por quase duas décadas de demonização da marijuana e dos indivíduos que a consumiam. Mas no início dos anos 60, os desenvolvimentos na ciência e na sociedade estavam a provocar fissuras na muralha da proibição. As estruturas moleculares exactas do THC e do CBD foram determinadas em 1964 pelos cientistas israelitas Raphael Mechoulam e Y. Gaoni. Nesse ano, na cidade de Nova Iorque, Bob Dylan partilhou marijuana com os Beatles, pressagiando uma era em que milhões de jovens em todo o mundo – especialmente soldados e estudantes – começariam a fumar marijuana, a avaliar os seus efeitos por si próprios e a questionar as afirmações do governo.

O Dr. Mechoulam popularizou o termo “efeito de comitiva” para descrever como os compostos da Cannabis funcionam sinergicamente.
Evidências Anedóticas
Aqueles que começaram a fumar marijuana em ambientes sociais nos anos 60, 70 e 80 geralmente não sabiam que tinha sido amplamente prescrita como medicamento num passado não muito distante. Como disse o Dr. Mikuriya, “não foi só a marijuana que foi proibida, foi a verdade sobre a história”
Circulavam relatos anedóticos de eficácia médica. Aparentemente, toda a gente conhecia alguém no hospital VA que usava marijuana para a espasticidade, ou tinha uma tia que se safou da quimioterapia graças à erva, ou um amigo que dizia que o ajudava a dormir. Mas nenhum médico ou investigador estava a seguir os pacientes que usavam marijuana.
Em 1990, em resposta à epidemia de SIDA, um veterano do Vietname chamado Dennis Peron criou o San Francisco Cannabis Buyers Club. O clube proporcionou um ambiente em que as pessoas que usavam marijuana para fins medicinais podiam comparar notas e ter uma noção dos seus números. Mikuriya, vendo “uma oportunidade única de investigação”, assumiu o cargo de coordenador médico e começou a entrevistar os membros sobre as suas doenças, padrões de consumo de marijuana e resultados.
O notável clube de Peron tornou-se a sede dos activistas que trabalhavam para legalizar a marijuana para uso medicinal. Eles redigiram a “Proposta 215”, uma medida eleitoral que permitiria aos pacientes, com a aprovação de um médico, usar cannabis medicinalmente. Os eleitores da Califórnia aprovaram a Proposta 215 em novembro de 1996 por uma margem de 56% a 44% – contra a oposição das forças da ordem e de todos os eleitos do estado, à exceção de Terence Hallinan, procurador distrital de São Francisco.

Dennis Peron à porta do Clube de Compradores de Cannabis de São Francisco, no número 1444 da Market Street. Em 1995, o clube tornou-se o quartel-general dos activistas que planeavam a iniciativa de marijuana medicinal da Califórnia.

Os funcionários da Administração Clinton, liderados pelo Czar da Droga Barry McCaffrey, denunciaram Tod Mikuriya, MD, e ameaçaram os médicos que aprovaram o uso de marijuana pelos seus pacientes depois de os eleitores da Califórnia terem aprovado a Proposta 215 em novembro de 1996.
A pedido do Dr. Mikuriya, a nova lei foi redigida de modo a abranger não só os doentes que sofrem de algumas doenças graves, mas também aqueles que sofrem de “qualquer outra doença para a qual a marijuana proporcione alívio”
Em dezembro de 1996, o czar da droga dos EUA Barry McCaffrey e a Procuradora-Geral Janet Reno ameaçaram revogar as licenças de prescrição dos médicos da Califórnia que se atrevessem a aprovar o consumo de marijuana pelos pacientes. Numa conferência de imprensa amplamente divulgada, McCaffrey apontou de forma zombeteira para uma grande tabela intitulada “Usos Médicos da Marijuana do Dr. Tod Mikuriya (215 Medical Advisor)” McCaffrey disse que era um absurdo que uma droga pudesse ser eficaz no tratamento de tantas doenças. “Isto não é medicina”, ironizou, “é um espetáculo do Cheech e do Chong”
A União Americana das Liberdades Civis e o grupo reformista agora conhecido como Aliança para a Política de Drogas apoiaram um processo movido pelo especialista em SIDA Marcus Conant, MD, para impedir o governo de levar a cabo a sua ameaça. Os tribunais federais concordaram com os queixosos que os médicos e os pacientes têm o direito constitucional, ao abrigo da Primeira Emenda, de discutir a marijuana como uma opção de tratamento.

Cheech e Chong tornaram-se ícones da contracultura da canábis. Os seus filmes e as suas rotinas de comédia ignoravam os supostos perigos associados à marijuana.
O sistema endocanabinóide
Enquanto o conflito legal/político se desenrolava, os cientistas que estudam a forma como a canábis exerce os seus efeitos vieram dar razão a Mikuriya. Em 1990 – quando o Cannabis Buyers Club se estava a formar em São Francisco – um grupo de cientistas reuniu-se em Creta e lançou a International Cannabis Research Society. A palavra “C” no nome do grupo seria alterada para “Cannabinoid” em 1998 porque, como explicou um investigador, “o campo está a afastar-se da planta”
Os membros do ICRS eram na sua maioria farmacologistas e bioquímicos empregados em centros de investigação académicos. Quase todos receberam ou cobiçaram financiamento do Instituto Nacional de Abuso de Drogas dos EUA (NIDA), uma agência cujo objetivo declarado durante anos foi provar a nocividade da marijuana. O Santo Graal dos cientistas era uma droga que exercesse os efeitos benéficos da canábis sem causar qualquer psicoactividade.
Na sua busca por esse medicamento, os investigadores descobriram o sistema de sinalização endocanabinóide do corpo – compostos produzidos no corpo que activam receptores endógenos que também respondem aos canabinóides das plantas.
Os canabinóides predominantes nas plantas de Cannabis são o CBD e o THC. O CBD, que não é psicoativo, predomina no cânhamo – plantas cultivadas para fibra e/ou sementes. O CBD foi identificado no início dos anos 40 por Roger Adams, um químico da Universidade de Illinois, mas não chegou a descobrir a sua estrutura molecular exacta.
Após a descoberta dos endocanabinóides, o CBD e o THC passaram a ser designados por “fitocanabinóides” – compostos encontrados na planta, quase todos constituídos por 21 átomos de carbono em estruturas anelares e cadeias laterais, com átomos de hidrogénio e oxigénio ligados em diferentes pontos.
Até à data, foram identificados cerca de 100 fitocanabinóides, incluindo alguns biologicamente activos que podem ter potencial médico. (Alguns canabinóides são criados fugazmente quando o material da planta está a ser analisado, outros são criados por enzimas que metabolizam os compostos da planta)
Para além dos fitocanabinóides, a planta da Cannabis biossintetiza centenas de substâncias químicas que não lhe são exclusivas, algumas das quais são biologicamente activas – incluindo terpenos e flavonóides que proporcionam cheiro, sabor e cor. Foram encontrados três flavonóides que são exclusivos da canábis: canflavina-A, -B e -C.
Os canabinóides endógenos (“endo-“) são produzidos no nosso corpo para enviar sinais de uma célula nervosa para outra. Estes compostos nos animais precederam os canabinóides das plantas por ordem evolutiva
evolutiva. Os endocanabinóides e os fitocanabinóides exercem efeitos semelhantes quando testados em animais de laboratório: redução da dor, da temperatura corporal, da atividade espontânea e do controlo motor.
Os compostos sintéticos que exercem estes efeitos são também classificados como canabinóides. Em 1974, a Eli Lilly produziu nabilone, uma forma sintética de THC que foi comercializada como Cesamet (e reintroduzida anos mais tarde como Nabilone). Em meados dos anos 80, a Pfizer produziu um composto sintético, o CP-55940, que se revelou demasiado psicoativo para ser comercializado como medicamento. Mas ao contrário do THC, que não é solúvel em água e exerce um efeito fraco e fugaz, o CP-55940 pode ser manuseado em solução aquosa e liga-se durante tempo suficiente para revelar em que parte do corpo actua. Isto foi uma grande vantagem para a investigação.
A existência de receptores canabinóides no cérebro foi estabelecida em 1988 por William Devane, trabalhando no laboratório de Alynn Howlett na Universidade de St. Louis. Os receptores são proteínas incorporadas nas membranas celulares. Os endocanabinóides ou fitocanabinóides que se ligam a eles induzem uma cascata de eventos moleculares no interior das células.
Estes receptores, mais tarde designados por receptores CB1, concentram-se no cerebelo e nos gânglios basais (regiões responsáveis pelo controlo motor, o que pode explicar a razão pela qual a marijuana supostamente alivia a espasticidade muscular); no hipocampo (armazenamento da memória de curto prazo); e no sistema límbico (controlo emocional). Os canabinóides que actuam através dos receptores CB1 desempenham um papel nos processos de recompensa, cognição e perceção da dor, bem como no controlo motor.

a ‘Sour Tsunami’, criada por Lawrence Ringo no condado de Humboldt, é uma variedade com predominância de CBD. Ringo tornou as sementes estabilizadas amplamente disponíveis para utilizadores médicos.
Em 1992, um segundo recetor canabinóide foi encontrado em células do baço, glóbulos brancos e outras áreas “periféricas” do corpo. A descoberta do recetor CB2 renovou a esperança de que pudessem ser desenvolvidas drogas não psicoactivas eficazes que envolvessem o sistema imunitário – e não o cérebro ou o sistema nervoso central.
Também em 1992, Devane e Lumir Hanas, que trabalhavam no laboratório de Mechoulam na Universidade Hebraica de Jerusalém, identificaram o primeiro canabinóide endógeno, uma molécula relativamente simples chamada N araquidonilanolamina (AEA). A anandamida actua nos receptores CB1 e CB2. Os seus efeitos são duplicados pelo THC. Também no laboratório de Mechoulam, em 1994, Shimon Ben-Shabat descobriu um segundo canabinóide endógeno, o 2-AG (2 arachidonoylglycerol), que também se liga aos receptores CB1 e CB2. Ao contrário da anandamida, que é um agonista relativamente fraco, o 2-AG é geralmente um agonista completo do recetor CB1.
A anandamida e o 2-AG são neuromoduladores invulgares na medida em que actuam através de um processo chamado “sinalização retrógrada” Os neurotransmissores convencionais – serotonina, dopamina, etc. – atravessam o espaço (sinapse) entre uma célula emissora “pré-sinápica” e uma célula recetora “pós-sinápica”. Os endocanabinóides são produzidos a pedido no neurónio pós-sináptico e reenviados através da sinapse para dizer à célula emissora para baixar ou acelerar o ritmo.
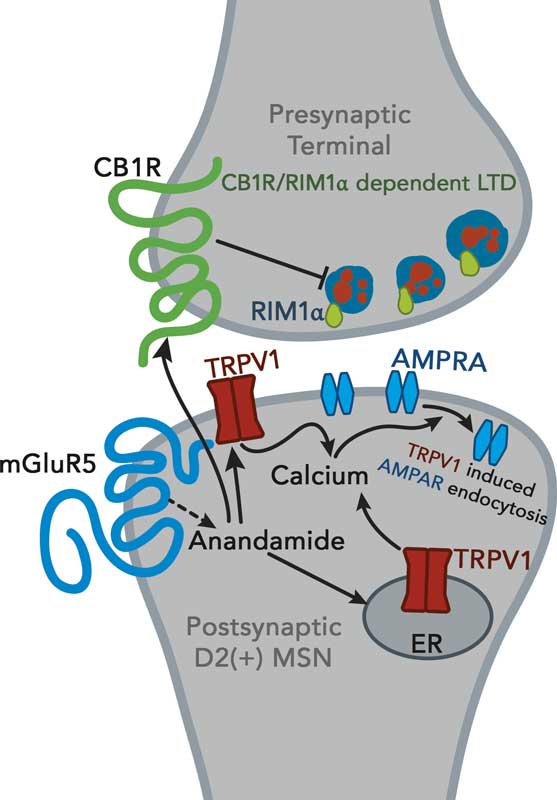
Uma célula nervosa envia sinais químicos através de um espaço – a sinapse – para ativar uma célula recetora. Os endocanabinóides são feitos a partir da membrana da célula recetora e enviados de volta através da sinapse para ajustar a taxa de transmissão.
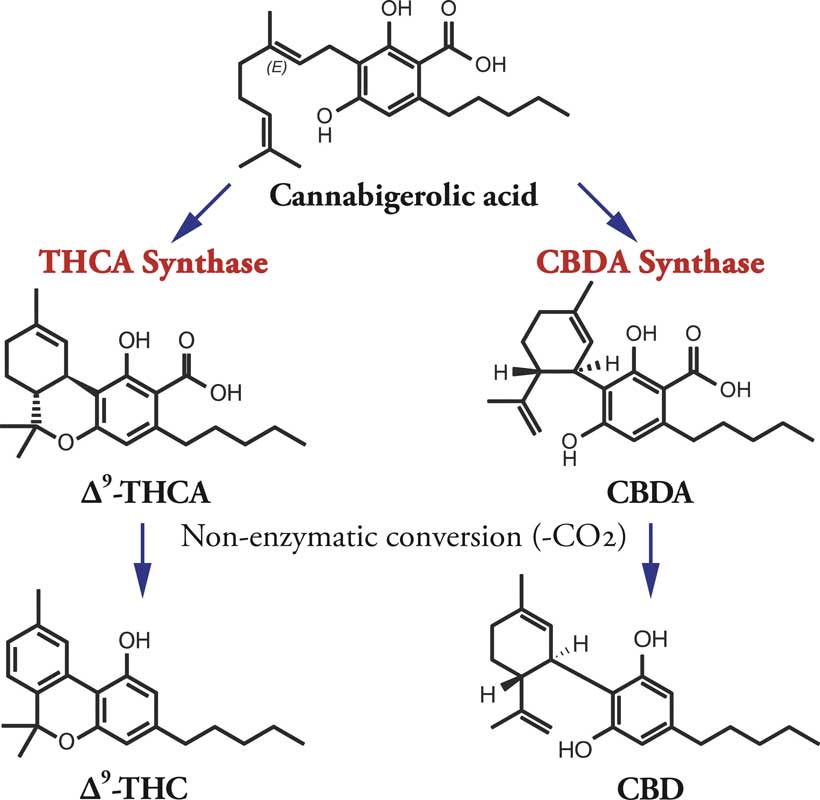
Os canabinóides vegetais têm 21 moléculas de carbono com oxigénio e hidrogénio ligados em vários locais.
A anandamida e o 2-AG restabelecem o equilíbrio – a homeostase – inibindo as células nervosas que disparam com demasiada intensidade e desinibindo as células nervosas que disparam com demasiada lentidão. Pensa num maestro que está de frente para uma orquestra e que dirige o ritmo e o volume a que os instrumentos produzem os seus sons. O sistema endocanabinóide é o
o sistema endocanabinóide é o mestre do tom do corpo.
Os endocanabinóides enviam os seus sinais de “manter o equilíbrio” nos sistemas que regulam o apetite, o movimento, a aprendizagem (e o esquecimento), a perceção da dor, a resposta imunitária e a inflamação, a neuroprotecção e outros processos vitais.
O facto de a sinalização endocanabinóide ser parte integrante de todos os processos fisiológicos explica por que razão a ingestão de canabinóides – inalação de vapor de canábis, por exemplo – pode beneficiar os pacientes que sofrem de qualquer um dos sintomas e condições médicas da infame lista de Tod Mikuriya. Os cientistas explicaram o que ele observou e relatou!
Na reunião de 2013 da Associação Internacional de Medicamentos Canabinóides, Raphael Mechoulam citou com aprovação um artigo que concluía que “a modulação da atividade endocanabinóide pode ter potencial terapêutico em quase todas as doenças que afectam os seres humanos”
Em cada reunião anual da Sociedade Internacional de Investigação de Canabinóides, tem-se dado mais ênfase às aplicações terapêuticas e menos à responsabilidade pelo abuso de drogas. Os estudos apresentados na reunião de 2014 reflectiram um interesse renovado na própria planta da canábis.
O que os médicos aprenderam
A iniciativa da Califórnia de 1996 relativa à marijuana medicinal não criou um sistema de registo porque Dennis Peron e os seus co-autores não queriam criar uma lista de utilizadores de canábis que os procuradores federais pudessem consultar se e quando quisessem. Assim, durante todos os anos que se seguiram, uma vasta experiência de saúde pública foi levada a cabo sem que nenhuma agência estatal a tivesse seguido.
Em 2006, dez anos após a legalização do uso medicinal, Mikuriya fez um inquérito a 30 médicos que tinham participado em reuniões do California Cannabis Research Medical Group (que ele tinha organizado em 2000). Publica os resultados na O’Shaughnessy’s, uma revista que co-fundou com um de nós (Fred Gardner) em 2003.
Cerca de 160.000 pacientes tinham sido autorizados a utilizar a erva pelos médicos inquiridos. Por unanimidade, os médicos ficaram impressionados com o facto de a canábis permitir aos pacientes reduzir a ingestão de medicamentos prescritos e de venda livre. Como diz Mikuriya: “Os opiáceos, os sedativos, os AINE e os antidepressivos SSRI são normalmente utilizados em quantidades mais reduzidas ou interrompidos. Todos estes medicamentos têm efeitos adversos graves”
O Dr. Robert Sullivan, um dos primeiros médicos a oferecer consultas sobre canábis em Orange County, na Califórnia, relatou que os seus pacientes tinham reduzido o consumo de “opiáceos, relaxantes musculares, antidepressivos, hipnóticos (para dormir), ansiolíticos, neurontina, anti-inflamatórios, medicamentos anti-enxaqueca, medicamentos gastrointestinais, prednisona (para asma, artrite)” A canábis estava a revelar-se o antidroga.
Relatos de doentes com dores que consomem canábis reduzem a ingestão de opiáceos em 50 por cento coincidem perfeitamente com estudos que mostram que os animais de laboratório precisam de metade dos opiáceos para obter alívio da dor quando também são tratados com um canabinóide. Será de admirar que os fabricantes de drogas sintéticas vejam o uso medicinal da canábis como uma ameaça às suas margens de lucro?
E quanto aos alegados efeitos adversos, incluindo a dependência, em que se baseia a proibição da marijuana? O Dr. Philip Denney disse sobre o inquérito de dez anos: “Praticamente nenhum foi relatado pelos pacientes, exceto os contactos com o sistema legal. Os doentes podem facilmente deixar de consumir canábis para passarem nos testes de despistagem de drogas ou quando viajam. A overdose de canábis comestível – uma sonolência desagradável que dura seis a oito horas – é rara e transitória.”
O Dr. Frank Lucido respondeu que a “diminuição da produtividade” levou dois doentes a deixarem de consumir canábis. Mas, acrescentou, “a esmagadora maioria refere que é mais produtiva quando os seus sintomas são controlados com canábis” Os empregadores devem tomar nota.

As flores de canábis disponíveis nos dispensários permitiram que os pacientes nos estados de marijuana medicinal reduzissem ou deixassem de usar produtos farmacêuticos sintéticos com efeitos secundários adversos.
A era do CBD
A aprovação da Proposta 215 na Califórnia incentivou pessoas de todo o mundo a pressionar pelo acesso à canábis medicinal. Em Inglaterra, os doentes com esclerose múltipla começaram a pressionar o Ministério da Saúde com maior urgência. Na primavera de 1997, os doentes de EM organizaram uma reunião pública em Londres que chamou a atenção do empresário farmacêutico Geoffrey Guy, MD, que se comprometeu a ajudá-los a atingir o seu objetivo.
Guy observou que a canábis que estava a ser utilizada em Inglaterra por doentes com esclerose múltipla e outros que relatavam benefícios médicos continha quantidades substanciais de CBD e de THC. A reduzida psicoactividade da canábis rica em CBD seria um ponto de venda fundamental quando ele apresentou ao Ministério do Interior o seu plano para produzir um medicamento de canábis de qualidade farmacêutica. A sua empresa, a GW Pharmaceuticals, foi devidamente licenciada para cultivar canábis para este fim na primavera de 1998.
Para obter aprovação para comercialização, os extractos da GW teriam de ser produzidos com uma consistência quase perfeita e demonstrar segurança e eficácia em ensaios clínicos. O primeiro passo de Guy foi comprar a coleção de plantas geneticamente diversificadas da Hortapharm, uma empresa holandesa fundada nos anos 80 pelos expatriados americanos David Watson e Robert Clarke.
Foram eles que tiveram a perceção de que o CBD e outros compostos para além do THC tinham efeitos significativos. Viajaram por todo o mundo recolhendo variedades de “raças terrestres”, algumas com quantidades substanciais destes canabinóides “menores” anteriormente ignorados” Watson e Clarke também compreenderam que os terpenóides que dão às variedades de canábis os seus aromas exerciam efeitos quando ingeridos.
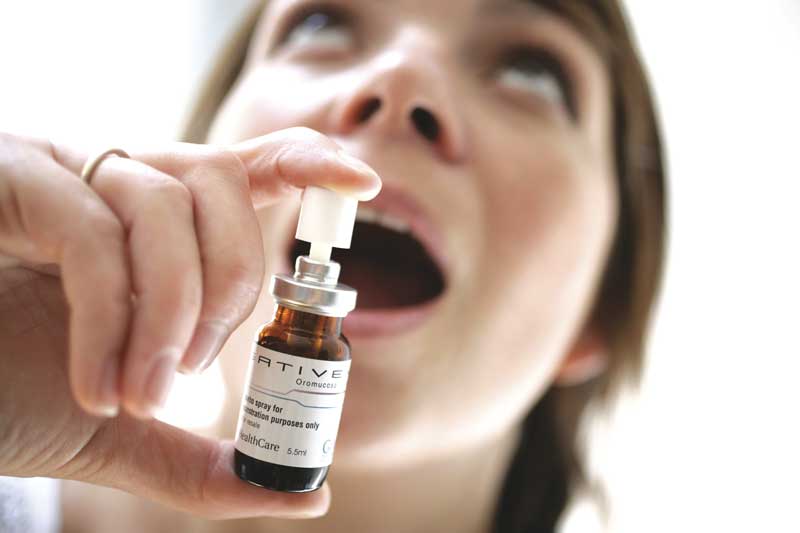
O Sativex da GW Pharmaceuticals, um spray de canabinóides sublingual, consiste em quantidades aproximadamente iguais de CBD e THC.
A GW começou a cultivar milhares de plantas em estufas sofisticadas no sudeste de Inglaterra. Além de desenvolver variedades com elevado teor de THC e CBD, a GW cultivou plantas ricas em canabicromeno (CBC), canabigerol (CBG) e tetrahidrocanabivarina (THCV) para testar os seus efeitos medicinais. Nos últimos anos, a canabidivarina (CBDV) tornou-se um composto de interesse para a empresa.
Em 1999, a GW estava a produzir o seu principal medicamento, o Sativex – um extrato de planta inteira formulado para ser pulverizado debaixo da língua. O Sativex contém quantidades aproximadamente iguais de CBD e THC, além de quantidades vestigiais de todos os outros compostos produzidos pela planta. A GW iniciou ensaios clínicos e começou a fornecer Sativex e outros extractos de canábis aos investigadores. As suas descobertas, relatadas em artigos de jornal e em conferências nos anos seguintes, sugeriram que o CBD poderia aliviar os sintomas de artrite reumatoide, diabetes, epilepsia, alcoolismo, PTSD, infecções resistentes a antibióticos e distúrbios neurológicos. O CBD também demonstrou efeitos neuroprotectores e anticancerígenos. As pessoas que usam Sativex diminuíram o uso de opiáceos e outros medicamentos. O Sativex produziu menos efeitos secundários e mais ligeiros do que o THC puro (Marinol).
Em abril de 2005, o Sativex obteve a aprovação condicional da Health Canada como tratamento para a dor na esclerose múltipla. O Reino Unido e cerca de 20 outros países aprovaram o Sativex para o tratamento da espasticidade na EM. O Sativex está atualmente a ser submetido a ensaios clínicos como tratamento para a dor do cancro nos EUA e noutros países.
Durante muitos anos, partiu-se do princípio de que o CBD tinha sido reduzido a níveis vestigiais em toda a canábis cultivada nos EUA para fins medicinais e recreativos. Como não havia laboratórios de química analítica a testar amostras de canábis, não havia forma de avaliar o teor de canabinóides. Esta situação mudou no inverno de 2008-2009, quando Steve DeAngelo, diretor do Harborside Health Center de Oakland, encorajou dois antigos cultivadores, David Lampach e Addison DeMoura, a lançar um laboratório, apropriadamente chamado Steep Hill.
O Harborside forneceu ao laboratório um fluxo constante de amostras para testar a presença de bolor e analisar os níveis de THC, CBD e CBN.
Descobriu-se que a canábis rica em CBD não era tão rara na Califórnia como os especialistas tinham previsto. A O’Shaughnessy’s informou que cerca de uma em cada 600 amostras trazidas para a Steep Hill e outros laboratórios em 2009 continha 4% ou mais de CBD. O ProjectCBD foi criado para informar o que médicos, pacientes, produtores e fabricantes estavam a aprender sobre medicamentos ricos em CBD.
P.S. (Post Sanjay)
Em agosto de 2013, Sanjay Gupta, MD, narrou um documentário na CNN no qual reconheceu que todos nós tínhamos sido “sistematicamente mal instruídos” sobre a marijuana. O programa apresentou exemplos dramáticos de efeitos benéficos da canábis. O mais memorável foi a história de uma criança de cinco anos, Charlotte Figi, que sofria de uma forma grave de epilepsia.
As convulsões de Charlotte tinham aumentado à medida que os tratamentos convencionais falhavam. A sua mãe, em Colorado Springs, e o seu pai, um sargento das Forças Especiais destacado no Afeganistão, pesquisaram na Internet e ficaram a saber que a canábis é um anticonvulsivo. Paige Figi obteve botões em dispensários e um amigo ensinou-a a extrair óleo para Charlotte. Uma variedade rica em CBD permitiu aliviar as convulsões, mas Paige não conseguiu reabastecer-se.

Wernard Bruining fundou o primeiro café em Amesterdão, o Mellow Yellow, em 1972. Atualmente, é a vanguarda holandesa da canábis medicinal. Visita o seu site, www.mediwiet.nl, para mais informações.
Foto de Lika Bruining.

Os Drs. Sanjay Gupta e Geoffrey Guy nas instalações de cultivo da GW Pharmaceuticals. A GW está a tentar obter a aprovação da FDA para o Sativex (para tratar a dor intratável do cancro) e o Epidiolex (para epilepsias pediátricas).
Em fevereiro de 2012, conheceu Joel Stanley, que, com os irmãos, cultivava marijuana para os seus próprios dispensários e tinha uma variedade de cânhamo que funcionava milagrosamente bem para Charlotte. Os Stanley mudaram o nome da sua planta para “Charlotte’s Web” e ofereceram-se para a cultivar em grandes quantidades para os Figis e outros necessitados. Quando Sanjay Gupta visitou a sua estufa, um dos irmãos Stanley apontou para uma planta Charlotte’s Web e afirmou: “Não há nada como isto no mundo. Esta planta tem 21% de CBD e menos de 1% de THC”
Felizmente, existem outras plantas de canábis com rácios de CBD:THC superiores a 20:1, e estão a ser cultivadas na Califórnia e noutros estados onde é legal fazê-lo. Também não é claro que quanto maior for o rácio CBD-THC, mais eficaz é o medicamento. Pode haver uma proporção ideal para tratar cada doença e cada indivíduo. O teor de terpenóides e flavonóides influenciará os efeitos de qualquer medicamento à base de canábis. Os médicos e os doentes, os cultivadores e os fabricantes de medicamentos têm uma oportunidade de investigação desafiante.
A lei federal Farm Bill de 2014 legalizou o cultivo de “cânhamo industrial” com 0,3 por cento de THC ou menos para fins de investigação. Isto permitiu aos irmãos Stanley cultivar 36.000 plantas de Charlotte’s Web – agora criadas para conter 30:1 de CBD para THC – em 17 acres, e redefinir o seu extrato como Óleo de Cânhamo CW. Vários milhares de plantas de cânhamo também foram cultivadas no Kentucky para uso medicinal. o “cânhamo industrial” está a fornecer mais do que alimentos e fibras. Foi apresentado no Congresso um projeto de lei para retirar o CBD e o cânhamo da Lei das Substâncias Controladas.
Centenas de pais de crianças com epilepsia, cancro e outras doenças graves mudaram-se para o Colorado na esperança de obter a Charlotte’s Web. Uma organização sem fins lucrativos chamada Realm of Caring, co-fundada por Paige Figi, aconselha famílias que estão a usar o produto dos irmãos Stanley, mantém uma lista de espera de potenciais clientes e actua como um recurso educacional. Em 2014, onze estados aprovaram projectos de lei que legalizam a canábis com quantidades mínimas de THC. Os proibicionistas vêem estes projectos de lei, chamados apenas de CBD, a desviar o apoio de projectos de lei que legalizariam o THC para uso medicinal (como aconteceu na Florida em novembro de 2014). Os defensores vêem-nos como um primeiro passo para uma legislação mais abrangente.
Várias empresas estão a produzir e a distribuir medicamentos à base de canábis nos EUA e no estrangeiro. As mais ousadas vendem produtos ricos em CBD pelo correio e online. Embora o CBD permaneça na Lista 1 da Lei Federal de Substâncias Controladas, os produtos alimentares de cânhamo com menos de 0,3% de THC são legais (e estão à venda na Costco).

Lawrence Ringo (à esquerda) e Jaime Carion (criador da ‘Cannatonic’, Resin Seeds) na High Times Medical Cannabis Cup em São Francisco. Ninguém fez mais para acelerar e expandir a disponibilidade de plantas ricas em CBD para uso médico do que estes dois homens.
Os reguladores federais não se opuseram às empresas que importam produtos médicos contendo grandes quantidades de CBD extraído de plantas de cânhamo cultivadas legalmente no estrangeiro. Os irmãos Stanley – que em 2014 foram aconselhados a não enviar o óleo de cânhamo Charlotte’s Web do Colorado para pacientes de outros estados – planeiam agora cultivar plantas no Uruguai e noutros países estrangeiros e enviar o óleo para pacientes nos EUA.
A GW Pharmaceuticals está a tentar obter a aprovação da FDA para o Epidiolex, um extrato de CBD desprovido de THC. O Epidiolex foi disponibilizado em 2014 a especialistas em epilepsia que conduziam programas de Investigação de Novos Medicamentos (IND) em hospitais nos EUA, envolvendo cerca de 200 crianças. Mais de metade das crianças tiveram convulsões significativamente menores e menos graves. Cerca de 15 por cento não tiveram qualquer ajuda e cerca de 15 por cento ficaram livres de convulsões. Um padrão semelhante foi relatado por Bonni Goldstein, MD, e Margaret Gedde, MD, médicos que tratam centenas de crianças usando cannabis rica em CBD para epilepsia em Los Angeles e Colorado Springs, respetivamente.
Martin Lee, organizador do Projeto CBD, afirma: “É irónico que a proibição da canábis, apresentada ao Congresso e a um público crédulo como uma forma de proteger as crianças de um vício mortal, esteja a desmoronar-se porque as crianças precisam urgentemente da canábis como medicamento.”
O grupo de médicos organizado por Tod Mikuriya em 2000, agora conhecido como Society of Cannabis Clinicians, tinha mais de 100 membros em junho de 2014. A SCC é dirigida desde 2009 por Jeffrey Hergenrather, médico, membro fundador. “Os conhecimentos dos médicos e dos doentes sobre o modo como a canábis funciona avançaram significativamente nos últimos anos”, afirma. “Agora está na altura de as escolas de medicina reconhecerem o sistema endocanabinóide”
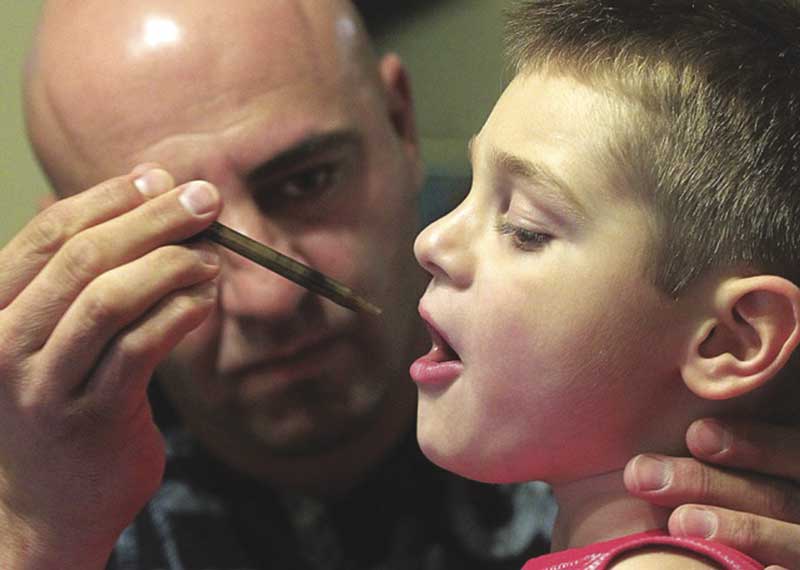
Jason David administrou o aceite rico em CBD do Harborside Health Center de Oakland ao seu filho Jayden, que lhe permitiu aliviar as convulsões. A notícia da melhora de Jayden inspirou os pais de Charlotte Figi a buscarem CBD no Colorado. Foto de Braverman Productions.
Ligações interessantes
O’Shaughnessy’s, cobre a história atual do movimento da marijuana medicinal.
ProjectCBD.org informa sobre a disponibilidade do CBD e o que cientistas, médicos, pacientes e produtores estão a aprender sobre ele.
The CBD Crew, uma parceria entre Mr. Nice e Resin Seeds, produz variedades ricas em CBD.

